
【题目】Na2S2O8具有强氧化性,在石油行业中有重要用途,工业上可利用电解法制备它,工作原理如图(电极材料是石墨)所示,且电子由外电路流入C2,下列说法正确的是
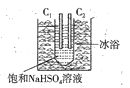
A. 阴极上的电极反应式为:2SO42--2e-=S2O82-
B. C1电极接电源负极,发生还原反应
C. 电解一段时间后,溶液的pH减小
D. 刚开始电解时,两电极上放电离子的物质的量相等
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】过氧硫酸氢钾复合盐(K2SO4·KHSO4·2KHSO5)易分解,可用作漂白剂、NOx和SO2等的脱除剂。某研究小组制备过氧硫酸氢钾复合盐的流程如下图:
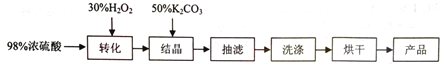
已知:浓硫酸与H2O2反应,部分转化为过氧硫酸(化学式为H2SO5,是一种一元强酸)
(1)若反应物的用量一定,在“转化”中为防止过氧化氢的分解,可采取的有效措施或操作有(写出两种)_____________、___________________。
(2)结晶操作中,加入K2CO3即可获得过氧硫酸氢钾复合盐晶体,该过程的离子方程式为____________。
过氧硫酸氢钾复合盐产率(以产品含氧量表示)随溶液pH和温度的变化关系如下图所示。则该过程适宜的条件是____________________。

(3)下列说法不正确的是______________________。
A.将晶体转移至布氏漏斗时,若器壁上粘有少量晶体,应用滤液淋洗
B.抽滤时,为防止滤纸穿孔,可适当关小水龙头或多加一层滤纸
C.用95%乙醇洗涤晶体目的是洗除晶体表面的杂质,易于得到干燥晶体
D.为加快产品的干燥,可高温烘干
(4)产品中KHSO5含量的测定:
取l.000g产品于锥形瓶中,用适量蒸馏水溶解,加入5mL10%的硫酸和10mL25%的碘化钾溶液,再加入2mL淀粉溶液作指示剂,用0.2000mol·L-1的硫代硫酸钠标准液滴定至终点,消耗标准液的体积为25.00 mL。
已知:2KHSO5+4KI+H2SO4=2I2+3K2SO4+2H2O
I2+2Na2S2O3=Na2S4O6+2NaI
则产品中KHSO5的质量分数为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃0.5 mol能与1 mol HCl完全加成,加成后产物分子上的氢原子又可与3 mol Cl2发生完全取代反应,则此气态烃可能是( )
A.C2H2B.CH2=CH2C.CH≡CCH3D.CH2=C(CH3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A. CH4与C4 H10 一定是同系物
B. 苯分子中既含有碳碳单键,又含有碳碳双键
C. 糖类、油脂、蛋白质都是天然高分子化合物
D. 淀粉和纤维素是同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向某密闭容器中加入X后会发生如下反应:5X(g) ![]() 2Y(g)+Z(g) ΔH<0,测得X的物质的量n(X)随时间t的变化如右图曲线Ⅰ所示,若改变某一条件后,向同种规格的密闭容器中加入等量的X后,测得n(X)随时间t的变化如右图曲线Ⅱ所示,下列说法错误的是
2Y(g)+Z(g) ΔH<0,测得X的物质的量n(X)随时间t的变化如右图曲线Ⅰ所示,若改变某一条件后,向同种规格的密闭容器中加入等量的X后,测得n(X)随时间t的变化如右图曲线Ⅱ所示,下列说法错误的是
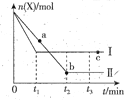
A. 曲线Ⅰ、曲线Ⅱ对应的反应只能是温度不同,且T(Ⅰ)>T(Ⅱ)
B. a、b、c三点对应的气体的平均相对分子质量:a>c>b
C. 平衡时Z的产率:b>c
D. t2-t3时间段内,两种条件下X的平均反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲除去下列物质中混入的少量杂质(括号内物质为杂质),不能达到目的的是( )
A.乙酸乙酯(乙酸):加入饱和Na2CO3溶液,充分振荡、静置后分液
B.乙醇(水):加入新制生石灰,蒸馏
C.乙酸(乙醇):加入氢氧化钠,充分反应后蒸馏
D.苯(液溴):加入NaOH溶液,振荡、静置分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年政府工作报告提出:继续坚定不移地打好包括污染防治在内的“三大攻坚战”。下列做法不符合这一要求的是( )
A. 推广新能源汽车,减少氮氧化物排放
B. 研发可降解塑料,控制白色污染产生
C. 直接灌溉工业废水,充分利用水资源
D. 施用有机肥料,改善土壤微生物环境
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com