
| A. | CO和CH3OH | B. | CO2和H20 | C. | H2和CO2 | D. | CH3OH和H2 |
分析 由题意知,绿色化学即环境友好型化学,其理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%,根据这一观点,要把一个C3H4分子变成一个甲基丙烯酸甲酯C5H802分子,还必须增加2个C原子、4个H原子、2个O原子,即原料中C、H、O的原子个数比为2:4:2,以此来解答.
解答 解:由题意知,绿色化学即环境友好型化学,其理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%,根据这一观点,要把一个C3H4分子变成一个甲基丙烯酸甲酯C5H802分子,还必须增加2个C原子、4个H原子、2个O原子,即原料中C、H、O的原子个数比为2:4:2.
A.CH3OH和CO,这两种物质如果按照分子个数比1:1组合,则很容易使C、H、O的原子个数比达到2:4:2,故A正确;
B.C02和H2O,其中两种物质里三种原子不论怎样组合也都不能使C、H、O的原子个数比为2:4:2,故B错误;
C.CO2和H2,两种物质分子里三种原子不论怎样组合也都不能使C、H、O的原子个数比为2:4:2,故C错误;
D.CH3OH和H2,其中两种物质分子里三种原子不论怎样组合都不能使C、H、O的原子个数比为2:4:2,故D错误;
故选A.
点评 本题考查绿色化学的概念,并以此为依据,考查元素种类、原子种类在化学变化中都保持不变,因此我们要用守恒的观点来解答,注意解本题时一定要读懂题意,明确命题者的意图,再结合所学方可解答,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | WX2分子中所有原子最外层都为8 电子结构 | |
| B. | WX2、ZX2的化学键类型相同 | |
| C. | WX2是以极性键结合成的分子 | |
| D. | 原子半径大小顺序为X<W<Y<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2的电子式: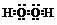 | B. | 磷原子的结构示意图: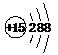 | ||
| C. | 乙醇的结构式:C2H6O | D. | 乙酸的结构简式:C2H4O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
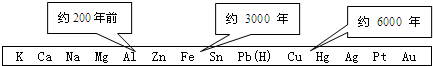
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
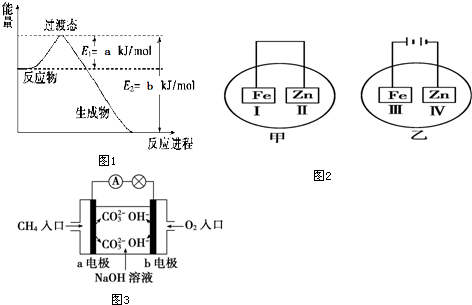
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com