
【题目】四种因素:①温度和压强 ②所含微粒数 ③微粒本身大小 ④微粒间的距离,其中对气态物质体积有显著影响的是( )
A. ②③④ B. ②④ C. ①③④ D. ①②④
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】CO2和甲烷催化合成CO和H2是CO2资源化利用的有效途径。主要反应为
Ⅰ:CH4(g)+CO2(g) ![]() 2CO(g)+2H2(g) △H=+247kJ/mol
2CO(g)+2H2(g) △H=+247kJ/mol
(1)已知CH4(g)+H2O(g) ![]() CO(g)+H2(g) △H=+206kJ/mol
CO(g)+H2(g) △H=+206kJ/mol
写出CH4和水蒸气反应生成CO2的热化学方程式_________。
(2)在恒温、恒容的密闭容器中发生反应I,下列选项能够说明反应I达到平衡状态的是______。
A.混合气体的密度不变
B.混合气体的总压强不变
C.CH4、CO2、CO、H2的物质的量之比为1:1:2:2
D.3V正(H2)=V逆(CH4)
E.混合气体的平均相对分子质量不变
(3)催化合成的温度通常维持在550-750℃之间,从反应速率角度分析其主要原因可能是_________。
(4)将CH4与CO2各1mol充入某密闭容器中,发生反应I。100Kpa时,反应I到达平衡时CO2的体积分数与温度的关系曲线如图所示。
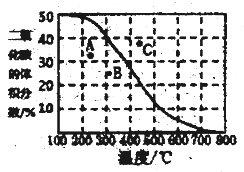
①图中A、B、C三点表示不同温度、压强下达到平衡时CO2的体积分数,则______点对应的平衡常数最小,判断依据是________;__________点对应的压强最大。
②300℃,100Kpa下,该容器中反应I经过40min达到平衡,计算反应在0-40min内的平均反应速率为v(CO2)=_________mol/min(结果保留两位有效数字),该温度下的压强平衡常数Kp=________。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
A. 工业上可用铝热反应大规模炼铁
B. SO2常用于纸张等植物纤维的漂白
C. Si是重要的半导体材料
D. 电解熔融MgCl2,可制得金属镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,调节反应物用量或浓度不会改变反应产物的是( )
A. CO2通入石灰水 B. AlCl3溶液中滴入NaOH溶液
C. NaHCO3溶液中滴入稀盐酸 D. 硫酸中加入锌粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.01mol氯化铬(CrCl3·6H2O)在水溶液中用过量的AgNO3溶液处理,产生0.02molAgCl沉淀,此氯化铬最可能为
A.[Cr(H2O)6]Cl3B.[Cr(H2O)4Cl2]Cl·2H2O
C.[Cr(H2O)5Cl]Cl2·H2OD.[Cr(H2O)3Cl3]·3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨及其相关工业中,部分物质间的转化关系如下:
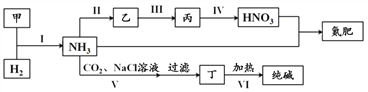
下列说法不正确的是( )
A. 甲、乙、丙三种物质中都含有氮元素
B. 反应II、III和Ⅳ的氧化剂相同
C. VI的产物可在上述流程中被再次利用
D. V中发生反应:NH3 + CO2 + H2O + NaCl === NaHCO3↓+ NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 常温常压下,11.2 L N2为0.5 mol
B. 标准状况下,22.4 L H2和O2的混合气体所含分子数为NA
C. 标准状况下,18 g H2O的体积是22.4 L
D. 1 mol SO2的体积一定为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下有三组混合物:①氯化钠和水;②硫酸钡和水;③煤油和水。分离以上混合液的正确方法依次是( )
A. 分液、萃取、蒸馏 B. 蒸发、过滤、分液 C. 分液、蒸发、萃取 D. 蒸馏、萃取、分液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com