
| A.若把H2S分子写成H3S分子,违背了共价键的饱和性 |
| B.晶体中若有阳离子一定有阴离子 |
| C.金属键存在于任何含金属元素的物质中 |
| D.晶体中一定存在化学键 |
 口算能手系列答案
口算能手系列答案科目:高中化学 来源:不详 题型:单选题
| A.全部 | B.②③④⑤⑥ | C.④⑤⑥ | D.⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2(g)的燃烧热为571.6 kJ·mol-1 |
| B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
| C.H2SO4(aq)+Ba(OH)2(aq)==BaSO4(s)+H2O(l)ΔH=-57.3 kJ·mol-1 |
| D.3H2(g)+CO2(g)=CH3OH(l)+H2O(l)ΔH=+135.9 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由极性键构成的极性分子 | B.由极性键构成的非极性分子 |
| C.由非极性键构成的极性分子 | D.由非极性键构成的非极性分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ·mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 |
| B.已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ·mol--1,则氢气的燃烧热为241.8 kJ·mol-1 |
| C.已知2C(s)+2O2(g)=2CO2(g)△H=a、2C(s)+O2(g)=2CO(g)△H=b,则a>b |
| D.已知P (白磷,s)=P (红磷,s)△H<0,则白磷比红磷稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
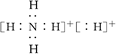 ,下列说法正确的是( )
,下列说法正确的是( )| A.NH5属于离子化合物 |
| B.NH5属于共价化合物 |
| C.NH5只含有离子键 |
| D.NH5只含有共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 N2 + H2O + nX(未配平的反应式)。
N2 + H2O + nX(未配平的反应式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com