
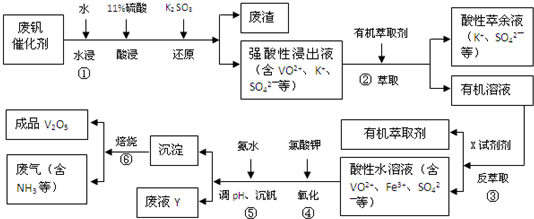
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| ��������/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
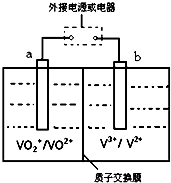
���� �Ϸ���������Ҫ�ɷ�V2O5��Fe2O3��SiO2�ȣ��������ʵ�ˮ����ȷ����V2O5��SiO2������ˮ����Ϊ�õ�����������������л�ԭ�ԣ����������£��ܱ���������������������������ӣ����ӷ�Ӧ����ʽΪ��V2O5+SO32-+4H+=2VO2++SO42-+2H2O�����˵õ�����Ϊ�������裬ǿ���Խ���Һ����VO2+��K+��SO42-�������л���ȡ����ȡ��Һ�õ��л���Һ��VO2+���ټ���X�Լ����з���ȡ��Һ��������л���õ�ˮ���Ǻ�VO2+��Fe3+��SO42-������ˮ��Һ���õ�����ƽ�⣬Rn+��ˮ�㣩+nHA���л��㣩?RAn���л��㣩+nH+��ˮ�㣩������ļ���ƽ���е������ӷ�Ӧ�ٽ�ƽ��������У�������������ƽ��������У�����ؾ��������ԣ��ܽ�VO2+����ΪVO2+�����백ˮ��������ҺpH�����ֵ���õ�NH4VO3������յõ�������������
��1������������֪����AΪ�������裻
��2������ȡʱ����ƽ�⣬VOSO4 +��ˮ�㣩+2HA2���л��㣩?VOA2���л��㣩+H2SO4��ˮ�㣩��Ϊ��ߢ�����ȡ�ٷ��ʣ��������к�����ʹƽ�����ơ����������ȡ������ȡ�������
��3������������ԭ��Ӧ�����غ�͵���غ㡢ԭ���غ���ƽ��д���ӷ���ʽ��
��4���ӳ����ʺ�pH��ϵ�ҳ���ѳ����ʣ�����������Ϊ93.1%ʱ������Fe��OH��3����������ʱ��ҺPH=2����������������Ũ�ȣ�����ܶȻ�����������Һ�������ӵ�Ũ�ȣ�
��5���������̷�Ӧ�����жϣ���ҺY�г�H+֮���������ΪFe3+��VO2+��NH4+��K+��
��6��������ͼ����ѭ�������ʣ������л���ȡ�����ڢ�����ȡ�����а������ڢ��е���pH��
��7�������ʱ���Ҳ���Һ��ɫ����ɫ��Ϊ��ɫ��˵���Ҳ�V3+����V2+��˵�����ʱ�Ҳ�Ϊ���������Ϊ��������ŵ�ʱ���Ϊ�������Ҳ�Ϊ�������ŵ�ʱ�������ϵķ�Ӧ��VO2++2H++e-�TVO2++H2O�������Ϸ���V2+-e-=V3+�ķ�Ӧ��
��� �⣺�Ϸ���������Ҫ�ɷ�V2O5��Fe2O3��SiO2�ȣ��������ʵ�ˮ����ȷ����V2O5��SiO2������ˮ����Ϊ�õ�����������������л�ԭ�ԣ����������£��ܱ���������������������������ӣ����ӷ�Ӧ����ʽΪ��V2O5+SO32-+4H+=2VO2++SO42-+2H2O�����˵õ�����Ϊ�������裬ǿ���Խ���Һ����VO2+��K+��SO42-�������л���ȡ����ȡ��Һ�õ��л���Һ��VO2+���ټ���X�Լ����з���ȡ��Һ��������л���õ�ˮ���Ǻ�VO2+��Fe3+��SO42-������ˮ��Һ���õ�����ƽ�⣬Rn+��ˮ�㣩+nHA���л��㣩?RAn���л��㣩+nH+��ˮ�㣩������ļ���ƽ���е������ӷ�Ӧ�ٽ�ƽ��������У�������������ƽ��������У�����ؾ��������ԣ��ܽ�VO2+����ΪVO2+�����백ˮ��������ҺpH�����ֵ���õ�NH4VO3������յõ�������������
��1������������֪���з�������Ҫ�ɷ��Ƕ������裬�ʴ�Ϊ��SiO2��
��2��������ȡʱ����������������ƽ�⣬Rn+��ˮ�㣩+nHA���л��㣩?RAn���л��㣩+nH+��ˮ�㣩������ļ���ƽ���е������ӷ�Ӧ�ٽ�ƽ��������У����з���ȡʱ�����X�Լ�������ƽ��������У����Լ�����������ƽ��������У�
�ʴ�Ϊ��������кͲ������ᣬƽ�����ƣ���߷�����ȡ�ʣ����
��3��ClO3-����Ԫ�ػ��ϼ�+5�۱仯Ϊ-1�ۣ�VO2+�仯ΪVO3+��VԪ�ػ��ϼ�+4�۱仯Ϊ+5�ۣ������غ�VO2+��VO3+ ��ϵ��Ϊ6��ClO3-�к�Cl-ǰϵ��Ϊ1����ϵ���غ��ԭ���غ���ƽ��д���ӷ���ʽΪ��ClO3-+6VO2++6H+=6VO3++Cl-+3H2O��
�ʴ�Ϊ��1��6�� 6��6��1 Cl-��3 H2O��
��4���ӳ����ʺ�pH��ϵ��֪����pH����������������С���ʳ���������pH��Ϊ���pH��pH=1.7ʱ���ij��������Ϊ98.8%�����백ˮ������Һ�����pHΪΪ1.7������������Ϊ93.1%ʱ������Fe��OH��3����������ʱ��ҺPH=2����������������Ũ��c��OH-��=10-12mol/L��k[Fe��OH��3]=2.6��10-39=c��Fe3+��c3��OH-����c��Fe3+��=$\frac{2.6��1{0}^{-39}}{��1{0}^{-12}��^{3}}$=2.6��10-3mol/L��
�ʴ�Ϊ��1.7��2.6��10-3��
��5���������̷�Ӧ������������Լ��ڷ�Ӧ���������ɵ�����Ϊ����H+֮���������ΪFe3+��VO22+��NH4+��K+��
�ʴ�Ϊ��Fe3+��VO3+��NH4+��K+����д���ּ��ɣ���
��6��������ͼ��֪�������л���ȡ�����ڢ�����ȡ�����а������ڢ��е���pH���ʴ�Ϊ���л���ȡ������ˮ����������
��7���ٵ����ʱ���Ҳ���Һ��ɫ����ɫ��Ϊ��ɫ��˵���Ҳ�V3+����V2+��˵�����ʱ�Ҳ�Ϊ���������Ϊ��������ŵ�ʱ���Ϊ�������Ҳ�Ϊ�������ŵ�ʱ�������ϵķ�Ӧ��VO2++2H++e-�TVO2++H2O�������Ϸ���V2+-e-=V3+�ķ�Ӧ����Ӧ�ɱ�ʾΪVO2++V2++2H+ $?_{���}^{�ŵ�}$VO2++H2O+V3+��
�ʴ�Ϊ��VO2++V2++2H+ $?_{���}^{�ŵ�}$VO2++H2O+V3+������
�ڷŵ�����У�a��Ϊ����������VO2++2H++e-�TVO2++H2O���������⣬�ŵ�ʱ�����Һ��ɫ�ɻ�ɫ��Ϊ��ɫ����VO2++2H++e-�TVO2++H2O�������õ��ӵĻ�ԭ��Ӧ�����Դ˵缫�����������ӽ���Ĥ������������ͨ���ĸ�Ĥ���ŵ�ʱ�������ϵķ�Ӧ��VO2++2H++e-�TVO2++H2O�������Ϸ���V2+-e-=V3+�ķ�Ӧ����ת��1.0mol����ʱ����1.0mol H+���Ҳ��ƽ���ۣ�
�ʴ�Ϊ��VO2++2H++e-=VO2++H2O���ң���
���� ���⿼�������̷����жϣ��������ʺ�ʵ����Ƶķ���Ӧ�ã�Ϊ�߿��������ͣ�������ѧ���ķ�����ʵ��ͼ��������Ŀ��飬��Ŀ���漰������ԭ��Ӧ��ƽ���ܶȻ����㣬�����Ϣ�����ж�������ע�����ʵ�鷽������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��5.85gNaCl��������100mLˮ�У��Ƶ�0.1mol/L��NaCl��Һ | |
| B�� | ��25g��ˮCuSO4����ˮ�Ƴ�100mL��Һ����Ũ��Ϊ1mol/L | |
| C�� | ��wg a%��NaCl��Һ������$\frac{w}{2}$gˮ���õ�2a%��NaCl��Һ | |
| D�� | ��1���c1mol/L��������4���ˮϡ�ͣ�ϡ��Һ��Ũ��Ϊ0.2c1mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �˵��Ϊ12��ԭ�� | B�� | ������Ϊ8��ԭ�� | ||
| C�� | K��Ϊ�����ʱ��2�����ӵ�ԭ�� | D�� | �˵����Ϊ9��ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������������������ԭ��Ӧ�������� | |
| B�� | �廯������ȶ��Աȵ⻯������ȶ��Բ� | |
| C�� | KI������Һ����ˮ��Ӧ��֤����Ľ����Աȵ�Ľ���ǿ | |
| D�� | I2O5��Br2O5��ˮ��Ӧ���ɶ�Ӧ�ĸ�±�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ijѧϰС��Χ�����������ϵ��ʵ�飮
ijѧϰС��Χ�����������ϵ��ʵ�飮| A | B | C | D | |
| �� | �������ɫ���� | �������ɫ���� | ʪ�����ɫ���� | ʪ�����ɫ���� |
| �� | ��ʯ�� | �轺 | Ũ���� | ��ˮ�Ȼ��� |
| �� | ʪ�����ɫ���� | ʪ�����ɫ���� | �������ɫ���� | �������ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
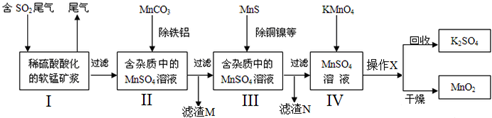
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ�ͷ����ܵõ�ʯ���������ͺ�ú�͵������Դ | |
| B�� |  ����ͼѭ��ת�������У�̫��������ת��Ϊ���� | |
| C�� | ú�ĸ�����ָ��ú�ڿ����м��ȵĹ��̣���ҵ��Ҳ��ú�Ľ��� | |
| D�� | ���ࡢ��֬����������Ϊ������������ṩ�����Ļ���Ӫ�����ʣ����ܷ���ˮ�ⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com