
| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| æŖŹ¼³ĮµķŹ± | 1.5 | 3.3 | 6.5 | 9.4 |
| ³ĮµķĶźČ«Ź± | 3.7 | 5.2 | 9.7 | 12.4 |
·ÖĪö £Ø1£©²½Öč¢ņÖŠ¼ÓČėŹŹĮæµÄH2O2£¬½«ČÜŅŗÖŠFe2+Ńõ»Æ³ÉFe3+£¬ŌŁµ÷½ŚČÜŅŗpHÖĮ7”«8£¬¼ÓČėŹŌ¼ĮŗĶĖį·“Ó¦ĢįøßČÜŅŗpH£¬Ź¹Fe3+”¢Al3+µČŌÓÖŹĄė×Ó³Įµķ·ÖĄė³żČ„£¬ŹŌ¼Į²»ÄÜŅżČėŠĀµÄŌÓÖŹ·ÖĪö£»
£Ø2£©¢Ł²½Öč¢óÖŠÖʱøĒāŃõ»ÆĆ¾ŹĒÓĆ°±Ė®³ĮµķĆ¾Ąė×Ó£¬×¢ŅāŅ»Ė®ŗĻ°±ŹĒČõµē½āÖŹ£»
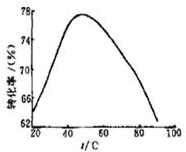
50”ęĒ°ĪĀ¶ČÓėMg2+×Ŗ»ÆĀŹÖ®¼äµÄ¹ŲĻµŹĒ£ŗĖęĪĀ¶ČÉżøßĆ¾Ąė×Ó×Ŗ»ÆĀŹŌö“󣬷“Ó¦ŹĒĪüČČ·“Ó¦£»
¢ŚĪĀ¶ČÉżøßÖĮ50”ęŅŌÉĻMg2+×Ŗ»ÆĀŹĻĀ½µµÄæÉÄÜŌŅņŹĒĪĀ¶Č¹żøߏ±£¬°±Ė®ŹÜČČ·Ö½ā£¬ÅØ¶Č½µµĶ£¬Mg2+×Ŗ»ÆĀŹĻĀ½µ£®
½ā“š ½ā£ŗ£Ø1£©²½Öč¢ņÖŠ¼ÓČėŹŹĮæµÄH2O2£¬½«ČÜŅŗÖŠFe2+Ńõ»Æ³ÉFe3+£¬ŌŁµ÷½ŚČÜŅŗpHÖĮ7”«8£¬¼ÓČėŹŌ¼ĮŗĶĖį·“Ó¦ĢįøßČÜŅŗpH£¬Ź¹Fe3+”¢Al3+µČŌÓÖŹĄė×Ó³Įµķ·ÖĄė³żČ„£¬ŹŌ¼Į²»ÄÜŅżČėŠĀµÄŌÓÖŹ£¬
A£®¼ÓČėŃõ»ÆĆ¾ŗĶĖį·“Ó¦ÄÜĢįøßČÜŅŗpH£¬Éś³ÉĆ¾Ąė×Ó£¬²»¼ÓČėŌÓÖŹĄė×Ó£¬æÉŃ”£»
B£®¼ÓČėĢ¼ĖįÄĘÄܵ÷½ŚČÜŅŗpH£¬µ«ŅżČėÄĘĄė×Ó£¬¹Ź²»Ń”£»
C£®ÕōĮóĖ®²»ÄÜŹ¹ČÜŅŗÓÉĖįŠŌ±äĪŖ¼īŠŌ£¬¹Ź²»Ń”£»
D£®¼ÓČėNaOHÄܵ÷½ŚČÜŅŗpH£¬µ«ŅżČėÄĘĄė×Ó£¬¹Ź²»Ń”£»
¹Ź“š°øĪŖ£ŗ½«Fe2+Ńõ»Æ³ÉFe3+£»A£»
£Ø2£©¢Ł°±Ė®³ĮµķĆ¾Ąė×ÓÉś³ÉĒāŃõ»ÆĆ¾³Įµķ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗMg2++2NH3•H2OØTMg£ØOH£©2”ż+2NH4+£¬
øł¾ŻĶ¼ÖŠĖłŹ¾£¬50”ęĒ°ĪĀ¶ČÓėMg2+×Ŗ»ÆĀŹÖ®¼äµÄ¹ŲĻµŹĒ£ŗĖęĪĀ¶ČÉżøßĆ¾Ąė×Ó×Ŗ»ÆĀŹŌö“󣬷“Ó¦ŹĒĪüČČ·“Ó¦£»
¹Ź“š°øĪŖ£ŗMg2++2NH3•H2OØTMg£ØOH£©2”ż+2NH4+£»ĪüČČ£»
¢ŚĶ¼ÖŠĪĀ¶ČÉżøßÖĮ50”ęŅŌÉĻMg2+×Ŗ»ÆĀŹĻĀ½µµÄæÉÄÜŌŅņŹĒ£ŗĪĀ¶Č¹żøߏ±£¬°±Ė®ŹÜČČ·Ö½ā£¬ÅØ¶Č½µµĶ£¬Mg2+×Ŗ»ÆĀŹĻĀ½µ£¬
¹Ź“š°øĪŖ£ŗĪĀ¶Č¹żøߏ±£¬°±Ė®ŹÜČČ·Ö½ā£¬ÅØ¶Č½µµĶ£¬Mg2+×Ŗ»ÆĀŹĻĀ½µ£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹÖʱø·½°ø£¬Éę¼°ĪļÖŹ·ÖĄėĢį“攢Ąė×Ó³ĮµķµÄĢõ¼žŃ”Ōń”¢»ÆŃ§Ę½ŗāµÄÓ°ĻģŅņĖŲ”¢Ąė×Ó·½³ĢŹ½µÄŹéŠ“”¢³Įµķ×Ŗ»ÆµÄŌĄķÓ¦ÓĆ£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶŹµŃéÄÜĮ¦µÄ漲飬ÄѶČÖŠµČ£®


 ×÷Ņµøص¼ĻµĮŠ“š°ø
×÷Ņµøص¼ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | N2£ŗ | B£® | NH3 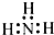 | C£® | H2O H+[£ŗO£ŗ]2-H+ | D£® | NaCl  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HI”¢HBr”¢HCl”¢HF | B£® | HCl”¢H2S”¢PH3”¢SiH4 | ||
| C£® | H2O”¢H2S”¢HCl”¢HBr | D£® | HF”¢H2O”¢PH3”¢NH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚŌŖĖŲÖÜĘŚ±ķĄļ£¬Ö÷×åŌŖĖŲĖłŌŚµÄ×åŠņŹżµČÓŚŌ×ÓŗĖĶāµē×ÓŹż | |
| B£® | ŌŚŌŖĖŲÖÜĘŚ±ķĄļ£¬ŌŖĖŲĖłŌŚµÄÖÜĘŚŠņŹżµČÓŚŌ×ÓŗĖĶāµē×Ó²ćŹż | |
| C£® | ×īĶā²ćµē×ÓŹżĪŖ8µÄĮ£×ÓŹĒĻ”ÓŠĘųĢåŌŖĖŲµÄŌ×Ó | |
| D£® | ŌŖĖŲµÄŌ×ÓŠņŹżŌ½“ó£¬ĘäŌ×Ó°ė¾¶Ņ²Ō½“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  AB2 | B£® |  EF2 | C£® |  XY3Z | D£® |  AB3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ”÷H=+88.6kJ•mol-1ŌņM”¢NĻą±Č£¬½ĻĪČ¶ØµÄŹĒM£®
”÷H=+88.6kJ•mol-1ŌņM”¢NĻą±Č£¬½ĻĪČ¶ØµÄŹĒM£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1£ŗ0.45 | B£® | 1£ŗ1 | C£® | 1£ŗ0.29 | D£® | 4.5£ŗ2.9 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | a+b£¼c+d£¬Q£¾0 | B£® | a+b£¾c+d£¬Q£¾0 | C£® | a+b£¼c+d£¬Q£¼0 | D£® | a+b=c+d£¬Q£¾0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Al2£ØSO4£©3 ČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®£ŗAl3++3OH-=Al£ØOH£©3”ż | |
| B£® | µē½ā±„ŗĶŹ³ŃĪĖ®£ŗ2Cl-+2H2O$\frac{\underline{\;µē½ā\;}}{\;}$H2”ü+Cl2”ü+2OH- | |
| C£® | Ģ¼ĖįøĘÓėŃĪĖį·“Ó¦£ŗCaCO3+2H+=Ca2++CO2”ü+H2O | |
| D£® | FeSO4 ČÜŅŗÖŠ¼ÓČėÓĆĮņĖįĖį»ÆµÄH2O2ČÜŅŗ£ŗFe2++H2O2+2H+=Fe3++2 H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com