
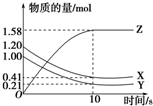
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是( )| A、反应开始到10s,用Z表示的反应速率为0.158mol/(L?s) |
| B、反应开始到10s,X的物质的量浓度减少了0.79mol/L |
| C、达平衡时Y的物质的量分数为:9.5% |
| D、反应的化学方程式为:X(g)+Y(g)?Z(g) |
| 1.58mol/2L |
| 10s |
| (1.20-0.41)mol |
| 2L |
| 0.21 |
| 2.20 |


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
| 电解质溶液 | 阳极 | 阴极 | 加入的物质 | |
| A | NaCl溶液 | 碳 | 铁 | 盐酸 |
| B | NaOH溶液 | 碳 | 碳 | 水 |
| C | 硫酸铜溶液 | 铜 | 碳 | 硫酸铜 |
| D | 硫酸 | 铁 | 碳 | H2O |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、积极开发风能发电和水力发电 |
| B、尽量用纯液态有机物代替水作溶剂 |
| C、提高原子利用率,发展绿色化学 |
| D、积极开发半导体节能灯具 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、达到平衡时X浓度为0.04 mol/L |
| B、将容器体积变为20 L,Z的平衡浓度变为0.015mol/L |
| C、若增大压强,平衡向正方向移动,平衡常数变大 |
| D、若升高温度,X的体积分数增大,则该反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4Cl溶液和HCl溶液的pH均小于7 |
| B、苯酚和氢氧化钠溶液在空气中久置均会变质 |
| C、铁片和铝片置于冷的浓硫酸中均无明显现象 |
| D、二氧化硫通入氯化钡溶液至饱和,再加入硝酸或苛性钠溶液都能产生白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③ | B、②③④ |
| C、①③ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(实验1中CO2的体积为标准状况下,其它气体在同温同压下测定).
如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(实验1中CO2的体积为标准状况下,其它气体在同温同压下测定). | 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
| 1 | 10mL 0.1mol/LNaOH溶液 | 22.4mLCO2 | 无明显现象 |
| 2 | 20mL H2S | 10mL SO2 | |
| 3 | 30mL NO2 | 10mL H2O(l) | 剩有无色气体,活塞自动向内压缩 |
| 4 | 15mL Cl2 | 40mL NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com