

分析 A是一种不溶于水的固体非金属氧化物,且A能够与纯碱(Na2CO3)、烧碱(NaOH)反应,A应该为SiO2;由转化关系可知B为Na2SiO3,C为CO2,D为H2SiO3,③为SiO2和NaOH的反应,Na2SiO3可与酸反应生成硅酸,硅酸加热分解生成二氧化硅,据此进行解答.
解答 解:A是一种不溶于水的固体非金属氧化物,且A能够与纯碱(Na2CO3)、烧碱(NaOH)反应,A应该为SiO2;由转化关系可知B为Na2SiO3,C为CO2,D为H2SiO3,③为SiO2和NaOH的反应,Na2SiO3可与酸反应生成硅酸,硅酸加热分解生成二氧化硅,
(1)由以上分析可知:A为SiO2,B为Na2SiO3,D为H2SiO3,
故答案为:SiO2;Na2SiO3;H2SiO3;
(2)①SiO2和碳酸钠在高温下反应生成硅酸钠和二氧化碳,反应的方程式为:Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑,
故答案为:Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑;
②硅酸酸性比碳酸弱,硅酸钠和二氧化碳、水反应可生成硅酸,反应的方程式为Na2SiO3+CO2+H2O═H2SiO3↓+Na2CO3,改成离子方程式为:CO2+H2O+SiO32-═CO32-+H2SiO3↓,
故答案为:CO2+H2O+SiO32-═CO32-+H2SiO3↓;
③二氧化硅和氢氧化钠反应生成硅酸钠和水,反应的化学方程式为SiO2+2NaOH═Na2SiO3+H2O,离子方程式为:SiO2+2OH-═SiO32-+H2O,
故答案为:SiO2+2OH-═SiO32-+H2O.
点评 本题考查无机物的推断,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,为高频考点,题目难度中等,本题主要侧重与含硅物质的综合考查,有利于提高学生的分析能力及逻辑推理能力.


科目:高中化学 来源: 题型:选择题
| A. | 密闭容器中,2mol SO2和1mol O2充分反应,生成SO3的分子数为2 NA | |
| B. | 1L1 mol•L-1 的(NH4)2SO4 溶液中含有的 NH4+数目为2NA | |
| C. | 足量的 MnO2与 100ml 12 mol•L-1的浓盐酸充分反应,转移的电子数目为 0.6 NA | |
| D. | 常温常压下,18 mL 水含有的分子数目约为 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 塑料、合成纤维、合成橡胶主要是以石油、煤和天然气为原料生产的 | |
| B. | 利用丁达尔效应可以提纯混有葡萄糖的稀淀粉溶液 | |
| C. | 氨气、二氧化碳、乙醇都属于非电解质 | |
| D. | 硫氧化物和氮氧化物是形成酸雨的主要物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H6和C5H12一定互为同系物 | |
| B. | 1mol葡萄糖与足量的金属钠反应,最多可生成2.5molH2 | |
| C. | 三氯甲烷只有一种结构证明甲烷是正四面体构型 | |
| D. | 油脂是食物中产生能量最高的营养物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
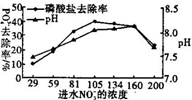 某文献报道可将ASBBR(一种生物膜反应器)用在有PO43-存在的环境中除磷,有一类微生物可在其中将PO43-还原为PH3,这项研究为解决含磷污染物的净化问题提供了新思路.某课题组在无氧环境中,用某腌制厂中含NO3-的废水对上述磷酸盐还原系统的除磷效率进行实验分析.
某文献报道可将ASBBR(一种生物膜反应器)用在有PO43-存在的环境中除磷,有一类微生物可在其中将PO43-还原为PH3,这项研究为解决含磷污染物的净化问题提供了新思路.某课题组在无氧环境中,用某腌制厂中含NO3-的废水对上述磷酸盐还原系统的除磷效率进行实验分析.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2+H2O═H2CO3 | B. | CO+CuO═Cu+CO2 | ||
| C. | 2H2O═2H2↑+O2↑ | D. | FeS+H2SO4═FeSO4+H2S↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ②③④ | C. | ②④⑥ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质名称 | 醋酸 | 氢氰酸 | 氢氟酸 | 甲酸 |
| 电离常数K | 1.75×10-5 | 4.93×10-10 | 7.2×10-4 | 1.77×10-4 |
| A. | 醋酸 | B. | 氢氰酸 | C. | 氢氟酸 | D. | 甲酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com