
| A. | 质子数:c>b | B. | 阴离子的还原性:Y2-<Z- | ||
| C. | 离子半径:X+>W3+ | D. | 氢化物的稳定性:H2Y>HZ |
分析 短周期元素离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,则有a-3=b-1=c+2=d+1,可知原子序数a>b>d>c,Y、Z为非金属,处于第二周期,故Y为O元素,Z为F元素,W、X为金属处于第三周期,W为Al元素,X为Na元素,结合元素周期律解答.
解答 解:X为Na、W为Al、Y为O、Z为F.
A.具有相同的电子层结构,b-1=c+2,则b=c+3,c<b,故A错误;
B.非金属性F>O,元素的非金属性越强,对应的阴离子还原性越弱,故B错误;
C.离子核外电子排布相同,核电荷数越大,离子半径越小,故C正确;
D.非金属性O<F,元素的非金属性越强,对应的氢化物越稳定,故D错误.
故选C.
点评 本题考查结构与位置关系、元素周期律等,为高频考点,侧重考查学生的分析能力,难度中等,根据电荷与核外电子排布相同推断元素在周期表中的位置是关键.


科目:高中化学 来源: 题型:选择题
| 容器 | 温度/k | 物质的起始浓度/mol•L-1 | CH3OH的平衡浓度/mol•L-1 | ||
| c(H2) | c(CO) | c(CH3OH) | |||
| Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
| Ⅱ | 400 | 0.40 | 0.20 | 0 | |
| Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
| A. | 该反应的正反应吸热 | |
| B. | 达到平衡时,容器II中c(CH3OH)小于容器I中c(CH3OH)的两倍 | |
| C. | 达到平衡时,容器II中c(H2)大于容器III中c(H2)的两倍 | |
| D. | 达到平衡时,容器III中的正反应速率比容器I中的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝可用于治疗胃酸过多 | B. | 甲醛可用作食品防腐剂 | ||
| C. | 铝制容器可以贮运浓硝酸 | D. | 过氧化钠可用作潜水艇供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 试剂 | 成分 | 价格/(元•吨-1) |
| 漂液 | 含25.2% NaClO | 450 |
| 双氧水 | 含30% H2O2 | 2400 |
| 浓硝酸 | 含98% HNO3 | 1500 |
| 氢氧化物 | 开始沉淀的pH | 沉淀完全的pH |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 4.0 | 6.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L已烷含有的共价键总数为19NA | |
| B. | 1mol Cu与足量FeCl3溶液反应,转移的电子数为2NA | |
| C. | 1L 0.1mol•-1 Na2CO3溶液中CO32-和HCO3-离子数之和为0.1NA | |
| D. | 密闭容器中1.5molH2与0.5molN2充分反应,得到NH3的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向含有FeI2的溶液中通入适量氯气,当有1mo1Fe2+被氧化时,该反应转移电子数目为3NA | |
| B. | 40gCuO和Cu2S混合物中所含铜原子的数目不等于0.5NA | |
| C. | 含0.1mo1NH4HSO4的溶液中,阳离子数目略小于0.2NA | |
| D. | C3H8分子中的2个H原子分别被1个-NH2和一个-OH取代,1mol此有机物所含共用电子对数目为13NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
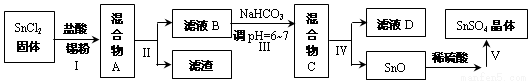
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、分液、萃取 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com