
| A、加硫酸铜溶液 |
| B、用同浓度的硫酸代替盐酸 |
| C、增大稀盐酸的用量 |
| D、不用铁片,改用铁粉 |
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
| A、共价化合物和离子化合物中,一定都含有非金属元素 |
| B、某元素原子最外层只有1个电子,它跟卤素可能形成离子键也可能形成共价键 |
| C、离子化合物如果能溶于水,其水溶液一定可以导电 |
| D、共价化合物都是由分子构成的,而离子化合物中一般不存在单个分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有共价键的化合物不一定是共价化合物 |
| B、单质分子中,一定存在着共价键 |
| C、含有离子键的化合物一定是离子化合物 |
| D、在共价化合物中,一定存在着共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
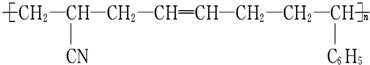 则生成该树脂的单体的种类和化学反应所属类型正确的是( )
则生成该树脂的单体的种类和化学反应所属类型正确的是( )| A、1种 加聚反应 |
| B、2种 缩聚反应 |
| C、3种 加聚反应 |
| D、3种 缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | ① | ② | ③ | ④ |
| 原子半径/10-10m | 0.74 | 1.60 | 1.52 | 1.10 |
| 主要化合价 | -2 | +2 | +1 | +5、-3 |
| 元素代号 | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/10-10m | 0.99 | 1.86 | 0.75 | 0.82 |
| 主要化合价 | +7、-1 | +1 | +5、-3 | +3 |
| A、上述八种元素最高价氧化物的水化物中,③号碱性最强 |
| B、上述八种元素最高价氧化物的水化物中,①号酸性最强 |
| C、②⑧不处于同一周期 |
| D、它们中气态氢化物的稳定性:⑦<④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔质量就等于物质的式量 |
| B、硫酸和磷酸的摩尔质量相等 |
| C、HNO3的摩尔质量是63g |
| D、摩尔质量就是物质式量的6.02×1023倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com