
用磁铁矿(主要成分Fe3O4、含Al2O3和SiO2等杂质),制取高纯铁红的工艺流程如下。
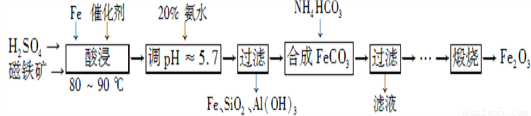
(1) 酸浸时,采用80-90℃的原因 _______________________________________________;
_______________________________________________;
铁粉的作用是____________________________________。
(2) 合成碳酸亚铁的离子方程式__________________________________________________________________。
(3) 图中“滤液”中主要阳离子是_______________________________________________________________;
(4)为了测定磁铁矿中铁的含量,称取80 g的磁铁矿样品加入足量稀硫酸使其充分溶解,过滤,得溶液100mL,取20mL溶液在酸性条件下用0.4 mol·L-1 KMnO4溶液滴定,当溶液中Fe2+ 全部被氧化时,消耗KMnO4溶液体积 10.00 mL。(已知MnO4-被还原为Mn2+)
mol·L-1 KMnO4溶液滴定,当溶液中Fe2+ 全部被氧化时,消耗KMnO4溶液体积 10.00 mL。(已知MnO4-被还原为Mn2+)
①写出滴定时反应的离子方程式__________________________________________
②当溶液中Fe2+ 全部被氧化时,c(Fe3+)=_____________________mol·L-1, (写出计算过程)。
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源:浙江省衢州市2017届高三1月教学质量检测化学试卷 题型:选择题
下列说法中,不正确的是
A. 碘单质升华,克服的是其分子间作用力
B. 金刚石、石墨、纳米碳管是碳元素的同素异形体
C. 目前科学家还无法实现对原子或分子的操纵
D. HCl气体溶于水后,共价键被破坏,从而形成了H+和Cl-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省南京市高二学业水平模拟测试化学试卷(解析版) 题型:选择题
工业上用 Co检查金属内部是否存在裂纹、气孔等。下列对的说法正确的是
Co检查金属内部是否存在裂纹、气孔等。下列对的说法正确的是
A. 核电荷数为27 B. 质子数为33 C. 中子数为60 D. 核外电子数为60
查看答案和解析>>
科目:高中化学 来源:2017届安徽省“江南十校”高三3月联考理综化学试卷(解析版) 题型:推断题
已知:①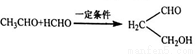 ②
②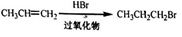
现用丙二酸等物质合成含有小环的有机物K,合成路线如下:
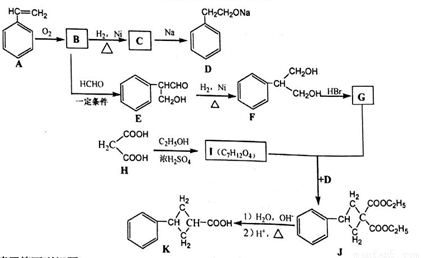
请回答下列问题:
(1)A的名称是_______,E中含氧官能团的名称是_____。
(2)B→C 的反应类型是_______ ,F→G的反应类型是____。
(3)G和I的结构简式分别为_______、________。
(4)写出F和H在一定条件下合成高分子化合物的化学反应方程式:_______。
(5)同时满足下列条件的E的同分异构体数目为________种。
① 能发生银镜反应;② 能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应。
(6)请写出以H2C=CHCH2Br为原料制备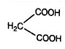 ,参考本题题干写出制备的合成线路流程图(无机试剂任选)。________
,参考本题题干写出制备的合成线路流程图(无机试剂任选)。________
查看答案和解析>>
科目:高中化学 来源:2017届安徽省“江南十校”高三3月联考理综化学试卷(解析版) 题型:选择题
用0.1000mol/L的标准盐酸分别滴定20.00mL的0.1000mol/L氨水和20.00mL的0.1000mol/L氢氧化钠溶液的滴定曲线如图所示,横坐标为滴定百分数(滴定用量/总滴定用量),纵坐标为滴定过程中溶液pH,甲基红是一种酸碱指示剂,变色范围为4.4-6.2,下列有关滴定过程说法正确的是
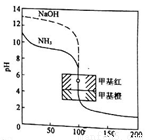
A. 滴定氨水溶液当滴定分数为50%时,各离子浓度间存在关系:c(NH4+)+c(H+)=c(OH-)
B. 滴定分数为100%时,即为滴定过程中反应恰好完全的时刻
C. 从滴定曲线可以判断,使用甲基橙作为滴定过程中的指示剂准确性更佳
D. 滴定氨水溶液当滴定分数为150%时,所得溶液中离子浓度有大小关系c(Cl-)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省扬州市宝应县高二下学期学业水平测试(三)化学试卷(解析版) 题型:选择题
下列实验方法能达到实验目的的是
A. 用丁达尔现象区分氢氧化铁胶体与氯化铜溶液
B. 用淀粉溶液检验食盐溶液中是否存在IO3-
C. 用氯化钡溶液鉴别碳酸钠溶液与硫酸钠溶液
D. 进入煤矿矿井时用火把照明
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省扬州市宝应县高二下学期学业水平测试(三)化学试卷(解析版) 题型:选择题
下列有关物质的性质与应用的说法中,均正确的是
A. Fe3+具有氧化性,可溶解印刷电路板上的金属铜
B. 碳酸钡、硫酸钡均难溶于水,均可用作钡餐
C. 氧化铝具有很高的熔点,可用于制造熔融烧碱的坩埚
D. 二氧化硅具有半导体性能,可以制成光电池
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省哈尔滨市高二3月月考化学试卷(解析版) 题型:填空题
x A(g) +2B(s) y C(g); △H <0在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
y C(g); △H <0在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
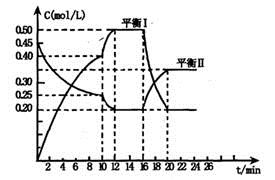
(1)用A的浓度变化表示该反应0~10min内的平均反应速率v(A)= ;
(2)根据图示可确定x:y= ;
(3)0~l0min容器内压强____ (填“变大”,“不变”或“变小”)
(4)推测第l0min引起曲线变化的反应条件可能是 ;第16min引起曲线变化的反应条件可能是____ ;
①减压;②增大A的浓度;③增大C的量;④升温;⑤降温;⑥加催化剂
(5)若平衡I的平衡常数为K1,平衡Ⅱ平衡常数为K2,则K1 K2(填“>”“=”或“<”)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省洛阳市高二(平行班)3月月考化学试卷(解析版) 题型:选择题
下列各组物质的晶体中,化学键类型相同,晶体类型也相同的是( )
A. CO2和SiO2 B. C60和Ar C. NaCl和HCl D. CaO和CsCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com