
【题目】苯和溴取代反应的实验装置如图所示,其中A为由具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉。填写下列空白:

(1)向反应容器A中逐滴加入溴和苯的混合液,几秒内就发生反应。写出A中所发生反应的化学方程式_______________________________________。
(2)B中NaOH溶液的作用是__________________。
(3)试管C中苯的作用是____________________________________。反应开始后,观察D和E两试管,看到的现象为____________________________,此现象可以验证苯和液溴的反应为__________(填反应类型)。
(4)在上述整套装置中,具有防倒吸作用的仪器有________(填字母)。
【答案】![]() 除去溶于溴苯中的溴 除去HBr气体中混有的溴蒸气 D试管中紫色石蕊试液慢慢变红,并在导管口有白雾产生,然后E试管中出现浅黄色沉淀 取代反应 DEF
除去溶于溴苯中的溴 除去HBr气体中混有的溴蒸气 D试管中紫色石蕊试液慢慢变红,并在导管口有白雾产生,然后E试管中出现浅黄色沉淀 取代反应 DEF
【解析】
(1)苯与溴在催化剂的作用下发生取代反应;
(2)溴单质易溶于溴苯,可以用氢氧化钠溶液洗涤除去;
(3)溴易挥发,易溶于有机溶剂,溴化氢溶于水电离产生氢离子和溴离子。
(1)苯与液溴在三溴化铁的催化作用下发生反应:![]() ;
;
(2)B中的氢氧化钠溶液作用是除去溶解在溴苯中的溴单质:Br2+2NaOH=NaBr+NaBrO+H2O;
(3)溴易挥发,易溶于有机溶剂,所以用苯来吸收溴化氢中的溴单质,防止对溴化氢的检验造成干扰;溴化氢溶于水完全电离,产生氢离子和溴离子,所以溶液显强酸性,能使石蕊变红色,在导管处能看到有白雾产生,硝酸银溶液中的银离子与溴离子反应生成了淡黄色沉淀;上述现象可以验证苯和液溴的反应为取代反应;
(4)D、E试管中导管在液面上方,可防止液体倒吸,E装置倒扣的漏斗也可防止液体倒吸;


科目:高中化学 来源: 题型:
【题目】为研究硝酸的性质设计并完成如下实验:
a、某兴趣小组设计如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。

(1)实验前,关闭活塞 b,试管 d 中加水至浸没长导管口,塞紧试管 c 和 d 的胶塞,加热 c,其目的是__________
(2)在 d 中加适量 NaOH 溶液,c 中放一小块铜片,由分液漏斗 a 向 c 中加入2mL 浓硝酸,c 中反应的离子方程式___________________________________________;再由 a 向 c 中加 2mL 蒸馏水、写出 c 中可能进行的两个反应的化学方程式_______________________________________;________________________________________.
b、室温下,将铁片分别置于适量的稀 HNO3 和浓 HNO3 中(如图所示)。

(1)气球的作用是_____________________________________
(2)A中溶液最终变为浅绿色,发生反应的离子方程式是______________________
(3)B 中无明显变化,该同学进一步探究如下:假设①常温下铁与浓硝酸不反应。②_______________________
进行实验:将 B 中的铁片取出并洗净后,放入 CuSO4 溶液中,无明显变化, 则说明假设①_____________(填“成立”或“不成立”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案中,能达到相应实验目的的是
A.方案①用于分离I2和NH4I固体
B.方案②用于比较CuSO4和MnO2的催化活性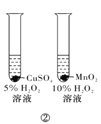
C.方案③用于测定中和热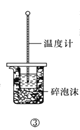
D.方案④用于比较醋酸和硼酸的酸性强弱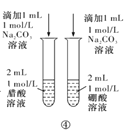
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形。RCl5在气态和液态时,分子结构如图所示,下列关于RCl5分子的说法中正确的是( )
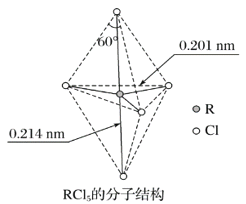
A. 每个原子都达到8电子稳定结构
B. 键角(Cl—R—Cl)有90°、120°、180°几种
C. RCl5受热后会分解生成分子RCl3,RCl5和RCl3都是极性分子
D. 分子中5个R—Cl键键能不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应方程式书写错误的是( )
A.![]() +HO-NO2
+HO-NO2![]()
![]() +H2O
+H2O
B.nCH2=CH2![]()
C.CH3COOH+CH3CH2OH![]() H2O+CH3COOCH2CH3
H2O+CH3COOCH2CH3
D.2CH3CH2OH+O2![]() 2CH3CHO
2CH3CHO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组设计如图所示的装置来验证元素非金属性的强弱:
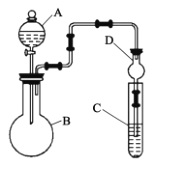
(1)仪器B的名称为___,干燥管D的作用是___。
(2)甲组同学的实验目的:证明非金属性:Cl>I。C中为淀粉—碘化钾混合溶液,B中装有KMnO4固体,则A中试剂为___,观察到C中溶液___(填现象),即可证明。但乙组同学认为该装置有明显的缺陷,改进方案是___。
(3)丙组同学的实验目的:证明非金属性:S>C>Si。在A中加稀硫酸、B中加Na2CO3溶液、C中加Na2SiO3溶液。观察到___(填现象),即可证明。C中发生反应的化学方程式为___。
(4)丁组同学的实验目的:证明非金属性:N>C>Si。实验方案与丙组同学的相似。在A中加稀硝酸、B中加Na2CO3溶液、C中加Na2SiO3溶液。观察到与丙组同学相同的实验现象,即可证明。但丙组同学认为该方案能证明非金属性:N>C,但不能证明非金属性:C>Si,理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】低碳经济是指在可持续发展理念指导下,尽可能地减少煤炭、石油等高碳能源消耗,减少温室气体排放,达到经济社会发展与生态环境保护双赢的一种经济发展形态。下列是有关碳元素的相关转化,回答下列问题:
(1)已知甲醇是一种清洁燃料,制备甲醇是煤液化的重要方向。若已知H2(g)、CO(g)、CH3OH(l)的燃烧热分别为H=-285.8kJ/mol、△H=-283.0kJ/mol、△H=-726.5kJ/mol,CO(g)+2H2(g)![]() CH3OH(l) △H=________ kJ/mol。
CH3OH(l) △H=________ kJ/mol。
(2)一定温度下,一定可以提高甲醇合成速率的措施有(______)
a.增大起始通入![]() 值
值
b.恒温恒容,再通入氦气
c.使用新型的高效正催化剂
d.将产生的甲醇及时移走
e.压缩体积,増大压强
(3)在恒温恒容条件下,下列说法可以判定反应CO(g)+2H2(g) ![]() CH3OH(g)已经达到平衡状态的是(______)
CH3OH(g)已经达到平衡状态的是(______)
a.体系中碳氢单键数目不再改变
b.体系中n(CO):n(H2)不再改变
c.体系中压强或者平均摩尔质量不再改变
d.单位时间内消耗氢气和CH3OH的物质的量相等
(4)在恒压的容器中,曲线X、Y、Z分别表示在T1°C、T2°C和T3°C三种温度下合成甲醇气体的过程。控制不同的原料投料比,CO的平衝转化率如图所示:
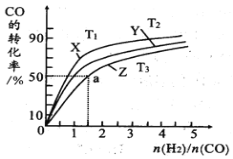
①温度T1°C、T2°C和T3°C由高到低的順序为:_________________;
②若温度为T3°C时,体系压强保持50aMPa,起始反应物投料比n(H2)/n(CO)=1.5,则平衡时CO和CH3OH的分压之比为__________,该反应的压强平衡常数Kp的计算式为__________。(Kp生成物分压幂的乘积与反应物分压幂的乘积的比值,某物质的分压等于总压强×该物质的物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最活泼的金属元素、最活泼的非金属元素、常温下呈液态的金属(价电子排布为5d106s2)元素分别位于下面元素周期表中的( )
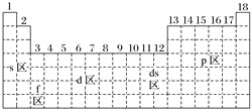
A. s区、p区、ds区 B. s区、p区、d区
C. f区、p区、ds区 D. s区、f区、ds区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是( )
A.苯和氯气生成![]() 的反应是取代反应
的反应是取代反应
B.乙烯与溴水发生加成反应的产物是![]()
C.等物质的量的甲烷与氯气反应的产物是![]()
D.![]() 的同分异构体的种数有 8种
的同分异构体的种数有 8种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com