
A、B和C为短周期非金属元素,原子序数依次减小,A的最低负化合价为-2,无最高正价,B是空气中含量最高的元素,C最外层电子数与电子层数相等。回答下列问题:
(1)A、B和C分别为__________、____________、_____________(用元素名称表示)。
(2)由以上元素组成的化合物中,属于离子化合物的是___________,属于共价化合物的是_________。(各写一种即可)
(3)B的常见气态氢化物的电子式为_______________,B的常见气态氢化物与其最高价氧化物对应的水化物反应产物的阳离子含有____________(填化学键的种类),该离子氯化物的水溶液呈__________性,用离子方程式表示为_______________________。
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源:2015-2016学年辽宁东北育才学校高二下第二段考化学试卷(解析版) 题型:选择题
某有机高分子由 、-CH2-CH2-两种结构单元组成,且它们自身不能相连,该烃分子中C、H两原子物质的量之比是( )
、-CH2-CH2-两种结构单元组成,且它们自身不能相连,该烃分子中C、H两原子物质的量之比是( )
A.1︰1 B.2︰1 C.2︰3 D.8︰7
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:推断题
现设计如下路线合成有机物E(C6H8O4),(其中A的相对分子质量是56,B的相对分子质量是125)。

(1)烃A的分子式是,D的结构简式为______________;
(2)③的反应类型是____________反应;
(3)已知E为顺式结构,则其结构简式是____________;
(4)下列说法正确的是____________(填序号)
a.反应①属于加成反应
b.B与二氯甲烷互为同系物
c.C存在立体异构体
d.D能使溴水褪色
(5)若C转化为D经过如下4步反应完成: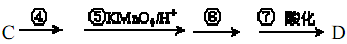 。
。
则④的化学方程式是____________,⑥所需的无机试剂及反应条件是____________。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:选择题
对下列物质的化学用语书写正确的是
A.乙烯的结构简式为CH2CH2
B.羟基的电子式:
C.Ca2+的结构示意图为
D.乙醇的分子式:CH3CH2OH
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前预测化学试卷(解析版) 题型:推断题
异苯丙醛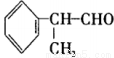 在工业上有重要用途,其合成流程如下:
在工业上有重要用途,其合成流程如下:
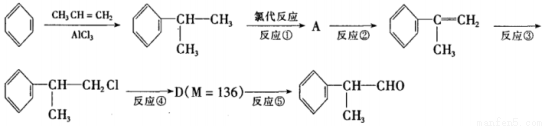
(1)异苯丙醛被酸性高锰酸钾氧化后所得有机物的结构简式是____________。
(2)在合成流程上②的反应类型是____________,反应④发生的条件是____________,
(3)反应⑤的化学方程式为____________。
(4)异苯丙醛发生银镜反应的化学方程式为__________。
(5)D物质与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,则X的名称是____________。D物质有多种同分异构体,其中满足苯环上有两个取代基,且能使FeCl3溶液显紫色的同分异构体有____________种。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前预测化学试卷(解析版) 题型:选择题
金属铜与浓硫酸反应的方程式中Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O。下列说法正确的是( )
A.Cu是氧化剂
B.H2SO4在反应中只表现氧化性
C.Cu在反应中被氧化
D.1mol氧化剂在反应中得到1mol电子
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前预测化学试卷(解析版) 题型:选择题
某学生对碱性工业废水样品进行研究,其实验操作或结论的描述,正确的是( )
A.将废水加入紫色石蕊试剂中检验酸碱性
B.用玻璃棒蘸取废水样品,蘸在润湿的pH试纸上测定其pH
C.测得该废水样品的pH=10,则废水样品中c(OH-)=10-10mol/L
D.该工业废水中c(H+)<c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三5月高考模拟理综化学试卷(解析版) 题型:实验题
焦亚硫酸钠(Na2S2O5)常用作食品漂白剂.其制备工艺流程如图:

已知:反应II包含2NaHSO3═Na2S2O5+H2O等多步反应。
(1)反应I的总化学方程式为____________,反应I进行时应先通入的气体是____________,反应I产生的NH4Cl可用作____________。
(2)灼烧时发生反应的化学方程式为____________,若灼烧时生 成SO21.12×l06 L(标准状况下),则转移电子____________mol.
(3)己知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为____________;
(4)副产品X的化学式是____________,在上述流程中可循环使用的物质是____________;
(5)为了减少产品Na2S2O5中杂质含量,需控制反应II中气体与固体的物质的量之比约为____________,检验产品中含有碳酸钠杂质所需试剂____________(填编号).
①澄清石灰水 ②饱和碳酸氢钠溶液 ③氢氧化钠 ④酸性高锰酸钾 ⑤稀硫酸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省汕头市高二下期末化学试卷(解析版) 题型:实验题
溴乙烷是有机合成的重要原料,实验室合成溴乙烷的装置示意图、相关原理和数据如下:
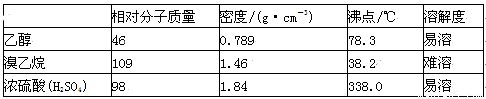
主反应:NaBr+H2SO4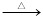 HBr+NaHSO4;C2H5OH+HBr
HBr+NaHSO4;C2H5OH+HBr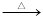 C2H5Br+H2O
C2H5Br+H2O
副反应:在该实验中经常会有乙醚、溴等副产物生成。
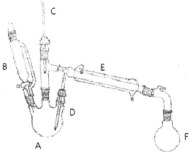
实验步骤:
①向A中先加入5 mL 95%的无水乙醇(0.085 mol)和4.5 mL的水,加入溴化钠7.725g,再加入沸石,摇匀。在接受器F中加冷水及3ml饱和亚硫酸氢钠溶液,并将其放入冰水浴中。
②在B中加入9.5 mL浓硫酸(0.17 mol),向A中缓缓滴入浓硫酸,加热体系,控制反应温度,保持反应平稳地发生,直至无油状物馏出为止;
③分出馏出液中的有机层,加入1-2 mL浓硫酸以除去乙醚、乙醇、水等杂质,溶液明显分层后,分离得到粗产物;
④将粗产物转入蒸馏瓶中,加沸石,在水浴上加热蒸馏,收集35-40℃的馏分,称量得5.23g。
回答问题:
(1)仪器A的名称为_________
(2)步骤①在接受器F中加冷水以及将F放入冰水浴中的目的是__________;饱和亚硫酸氢钠溶液的作用是________________
(3)步骤②中浓硫酸要缓缓滴加而不一次加入,其作用有________(填标号)。
a.可以防止乙醇发生碳化 b.避免生成HBr的速度过快,减少其挥发
c.避免溶液发生暴沸 d.减少因浓硫酸氧化HBr而生成副产物溴
(4)步骤③中分出馏出液中有机层的操作名称为________;加入浓硫酸除杂后的溶液明显分层,粗产物在________层(填“上”或“下”)。
(5)本实验的产率为________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com