
【题目】元素的性质与原子结构、元素在周期表中的位置有着密切的关系。回答下列问题:
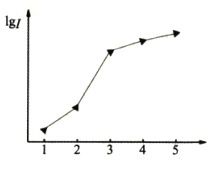
(1)如图表示某短周期元素X的前五级电离能(I)的对数值,试推测并写出X的元素符号___。
(2)化合物甲与SO2所含元素种类相同,两者互为等电子体,请写出甲的化学式___,甲分子中心原子的杂化类型是___。
(3)配位化学创始人维尔纳发现,将1mo1CoC13·5NH3(紫红色)和1mo1CoC134NH3(绿色)溶于水,加入AgNO3溶液,立即沉淀的AgCl分别为2mo1、1mol。则紫红色配合物中配离子的化学式为___,绿色配合物中Co的配位数为___。
(4)某稀土元素M的氧化物晶体为立方晶胞,其结构如图所示,图中小球代表氧离子,大球代表M离子。
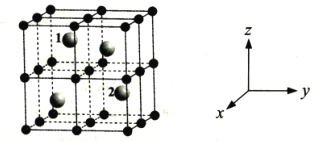
①写出该氧化物的化学式___。
②己知该晶体密度为ρg·cm-3,晶胞参数为anm,NA为阿伏加德罗常数的值。则M的相对原子质量Mr=___(用含ρ、a等的代数式表示);
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子1(M原子)的坐标为(![]() ,
,![]() ,
,![]() ),则原子2(M原子)的坐标为___。
),则原子2(M原子)的坐标为___。
【答案】Mg S2O或OS2 sp2 [Co(NH3)5Cl]2+ 6 MO2 ![]()
![]()
【解析】
(1)根据图像可以发现该元素的第三电离能显著增大,因此推测其为第二主族元素,而铍只有4个电子,不可能有第五电离能,因此只能为镁元素,其元素符号为![]() ;
;
(2)将一个氧原子换成一个硫原子,因此的甲的化学式为![]() 或
或![]() ,
,![]() 中硫原子是
中硫原子是![]() 杂化,考虑到等电子体的结构类似,因此
杂化,考虑到等电子体的结构类似,因此![]() 分子中心原子的杂化类型也为
分子中心原子的杂化类型也为![]() ;
;
(3)根据分析,1mol紫红色的物质中有2mol![]() 位于外界,因此剩下的1mol
位于外界,因此剩下的1mol![]() 位于内界,其配离子的化学式为
位于内界,其配离子的化学式为![]() ,而1mol绿色的物质中有1mol
,而1mol绿色的物质中有1mol![]() 位于外界,因此剩下的2mol
位于外界,因此剩下的2mol![]() 位于内界,因此其配位数为4+2=6;
位于内界,因此其配位数为4+2=6;
(4)①四个大球全部位于晶胞内部,因此按1个来算,而位于顶点的氧原子按![]() 来计算,位于棱心的氧原子按
来计算,位于棱心的氧原子按![]() 来计算,位于面心的氧原子按
来计算,位于面心的氧原子按![]() 来计算,位于体心的氧原子按1个来计算,因此一共有
来计算,位于体心的氧原子按1个来计算,因此一共有![]() 个氧原子,根据分析,一个晶胞内有4个M离子和8个氧离子,因此其化学式为
个氧原子,根据分析,一个晶胞内有4个M离子和8个氧离子,因此其化学式为![]() ;
;
②分子内有4个M和8个氧,因此一个晶胞的质量为![]() ,晶体的体积为
,晶体的体积为![]() ,代入
,代入![]() 后化简即可得到
后化简即可得到![]() ;
;
③把整个晶胞划分为8个小方块,则1号小球相当于左、上、后小方块的体心,2号小球相当于右、下、后小方块的体心,因此其坐标为![]() 。
。


科目:高中化学 来源: 题型:
【题目】某课外兴趣小组成员为研究金属铜与强酸的反应 ,将6.4g铜粉分为两等份,进行了如下实验,请完成有关计算。
(1)取其中一份铜粉投入200mL氢离子浓度为 1molL-1 硫酸和硝酸混合液中,微热使反应充分完成后,生成一氧化氮气体448mL(标准状况)。则反应前混合溶液中硫酸的物质的量浓度为_________(写出计算过程)。
(2)用NaOH溶液吸收氮氧化物是防止NO2污染的一种方法。原理为2NO2 + 2NaOH=NaNO3 + NaNO2 + H2O,NO + NO2 + 2NaOH=2NaNO2 + H2O。取另一份铜粉溶于过量的硝酸溶液,假设硝酸的还原产物只有一氧化氮和二氧化氮,生成的混合气体能被amol NaOH溶液完全吸收,试讨论a的取值范围:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇 广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性。下列关于白藜芦醇的说法正确的是
广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性。下列关于白藜芦醇的说法正确的是
A. 其核磁共振氢谱共有6组峰
B. 能够跟1mol该化合物起反应的Br2或H2的最大用量分别是5mol和7mol
C. 能分别与Na2CO3溶液、FeCl3溶液、NaHCO3溶液、酸性KMnO4溶液反应
D. 所有原子可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种具有强氧化性的黄绿色气体,也是优良的消毒剂,熔点-59℃、沸点11℃,易溶于水,易与碱液反应。ClO2浓度大时易分解爆炸,在生产和使用时必须用稀有气体或空气等进行稀释,实验室常用下列方法制备:2NaC1O3+Na2SO3+H2SO4![]() 2C1O2↑+2Na2SO4+H2O。
2C1O2↑+2Na2SO4+H2O。
(1)H2C2O4可代替Na2SO3制备ClO2,该反应的化学方程式为___,该方法中最突出的优点是___。
(2)ClO2浓度过高时易发生分解,故常将其制备成NaClO2固体,以便运输和贮存。
已知:2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O,实验室模拟制备NaC1O2的装置如图所示(加热和夹持装置略)。

①产生ClO2的温度需要控制在50℃,应采取的加热方式是___;盛放浓硫酸的仪器为:___;NaC1O2的名称是___;
②仪器B的作用是___;冷水浴冷却的目的有___(任写两条);
③空气流速过快或过慢,均会降低NaC1O2的产率,试解释其原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物D的一种合成路线如下:
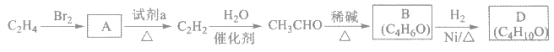
已知:![]()
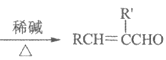 +H2O(R、R'表示烃基或氢)
+H2O(R、R'表示烃基或氢)
(1)由C2H4生成A的化学方程式是___________。
(2)试剂a是________。
(3)写出B中所含官能团的名称________。
(4)有机物D的结构简式是________。
(5)请以乙烯为起始原料,以CH3CH=CHCOOH为目标产物,结合已知信息选择必要的无机试剂,写出合成路线。_______(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物1-氧杂-2,4-环戊二烯(![]() )的说法正确的是()
)的说法正确的是()
A.![]() 与
与![]() 互为同系物
互为同系物
B.一氯代物有2种,二氯代物有4种(不考虑立体异构)
C.能使溴水退色,不能使酸性高锰酸钾溶液退色
D.1mol该有机物完全燃烧消耗5molO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟离子电池是一种前景广阔的新型电池,其能量密度是目前锂电池的十倍以上且不会因为过热而造成安全风险。如图是氟离子电池工作示意图,其中充电时F-从乙电极流向甲电极,下列关于该电池的说法正确的是( )

A.放电时,甲电极的电极反应式为Bi-3e-+3F-=BiF3
B.放电时,乙电极电势比甲电极高
C.充电时,导线上每通过1mole-,甲电极质量增加19g
D.充电时,外加电源的正极与乙电极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的结构如下图所示,下列说法中不正确的是( )
A. 在NaCl晶体 中,距Na+最近的Cl-有6个
中,距Na+最近的Cl-有6个
B.  气态团簇分子的分子式为EF或FE
气态团簇分子的分子式为EF或FE
C. 在CaF2晶体 中,每个晶胞平均占有4个Ca2+
中,每个晶胞平均占有4个Ca2+
D. 在金刚石晶体 中,碳原子与碳碳键个数的比为1∶2
中,碳原子与碳碳键个数的比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
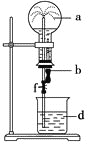
【题目】在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体d呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是
|
| |
A. |
| 水 |
B. |
| 4mol/LNaHSO3溶液 |
C. | Cl2 | 饱和NaCl水溶液 |
D. |
| 1mol/L盐酸 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com