
| A. | 氯化钠和金刚石 | B. | 二氧化硫和二氧化硅 | ||
| C. | 冰和干冰 | D. | 晶体硅和二氧化硅 |
分析 氮化硼是一种新合成的结构材料,它是一种超硬、耐磨、耐高温的物质,则氮化硼属于原子晶体,熔化时所克服的微粒间的作用力为共价键,然后判断选项中的晶体为原子晶体来解答.
解答 解:A.氯化钠熔化克服离子键,金刚石熔化克服共价键,故A不选;
B.二氧化硫为分子晶体,熔化克服的是分子间作用力,而二氧化硅是原子晶体,熔化克服共价键,故B不选;
C.冰和干冰都是分子晶体,熔化克服的是分子间作用力,故C不选;
D.晶体硅和二氧化硅都是原子晶体,熔化克服共价键,故D选;
故选D.
点评 本题考查晶体与化学键,明确不同类型晶体中的化学键是解答本题的关键,熟悉离子晶体中存在离子键,原子晶体中存在共价键即可解答,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:推断题
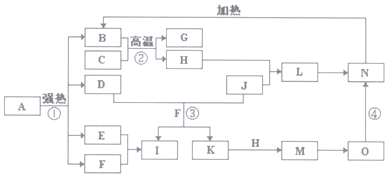
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 从海水中可提取食盐 | |
| B. | 海水蒸馏可得淡水 | |
| C. | 直接电解海水可得镁 | |
| D. | 从海水中得到淡水的方法有蒸馏法、电渗析法、离子交换法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
| 完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解熔融的氧化铝制取金属铝用铁作阳极 | |
| B. | 明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 | |
| C. | 在镀件上镀铜时可用金属铜作阴极 | |
| D. | 除去MgCl2溶液中的CuCl2既可用MgO也可用Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 研究NOX和CO等的处理方法对环境保护有重要意义.
研究NOX和CO等的处理方法对环境保护有重要意义. ①计算0~4分钟在A催化剂作用下,反应速率v(NH3)=0.25mol/(L•min).
①计算0~4分钟在A催化剂作用下,反应速率v(NH3)=0.25mol/(L•min).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知反应mA(g)+nB(g)?xC(g)+yD(g),A的转化率RA与p、T的关系如图,根据图示可以得出的正确结论是( )
已知反应mA(g)+nB(g)?xC(g)+yD(g),A的转化率RA与p、T的关系如图,根据图示可以得出的正确结论是( )| A. | 正反应吸热,m+n>x+y | B. | 正反应吸热,m+n<x+y | ||
| C. | 正反应放热,m+n<x+y | D. | 正反应放热,m+n<x+y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
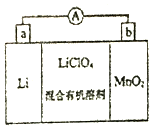 锰锂电池的体积小、性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题:
锰锂电池的体积小、性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com