
��֪����������Һ�м����������ʱ������Ӧ��4Fe2++4Na2O2+6H2O = 4Fe(OH)3��+O2��+8Na+��������˵����ȷ����
A���÷�Ӧ��Fe2+�ǻ� ԭ����O2�ǻ�ԭ����
ԭ����O2�ǻ�ԭ����
B��4molNa2O2�ڷ�Ӧ�й��õ�8NA������
C��Fe(OH)3���������ÿ����4molFe(OH)3��Ӧ�����й�ת�Ƶ���6mol
D����Ӧ�����п��Կ�����ɫ����ת��Ϊ����ɫ��ת��Ϊ���ɫ����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�߶��϶ο�����ѧ�Ծ��������棩 ���ͣ�ѡ����
25��ʱ����ˮ���������c(H+)��c(OH-)�ij˻�Ϊ1��10-18����Һ����ܴ����������������
A��NH4+��Na+��Cl-��I- B. Na+��K+��Fe3+��SCN-
C. Na+��Al3+��Cl-��AlO2- D. Na+��K+��Cl-��HCO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ��һ�Ͻο�����ѧ���������棩 ���ͣ������
Ҫ����������������
�ٱ���ʳ��ˮ��ɳ��
�ڴ�KNO3��NaCl�Ļ����Һ�л��KNO3
��ˮ�����͵Ļ����
��CCl4Һ����ױ�Һ��Ļ����(��֪CCl4��ױ����ܣ��е�ֱ�Ϊ76.75 ���110.6 ��)
(1)����ٵIJ���Ϊ____ ____��
(2)�����ʱ��ʹ����������һ�������������ʱ����ʹ�ã�����������_____ ___��
(3)�����������ʱ��ʹ�þƾ��Ƶ���____ ______��______ ______(�����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ��һ�Ͻο�����ѧ���������棩 ���ͣ�ѡ����
��������ԭ��Ӧ�����ֻ������ͷ�Ӧ�Ĺ�ϵ��ͼ��ʾ�������л�ѧ��Ӧ������Ӱ���ֵ���
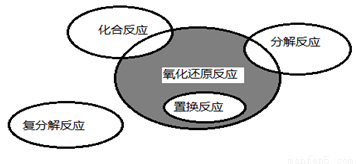
A��CO2��2Mg  C��2MgO
C��2MgO
B��2NaHCO3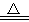 Na2CO3��H2O��CO2��
Na2CO3��H2O��CO2��
C��2Na2O2��2CO2===2Na2CO3��O2
D��4Fe(OH)2��O2��2H2O===4Fe(OH)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�츣��ʡ������ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ʵ����
ijѧ����������װ��̽�������백��֮��ķ�Ӧ������A��F�ֱ�Ϊ�����������ķ���װ�ã�CΪ��������������백����Ӧ��װ�á�
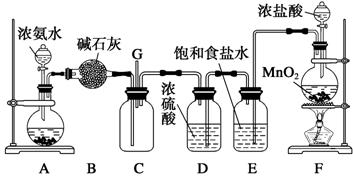
��1��װ��A�е���ƿ�ڹ��岻����ѡ�� ��ѡ����ţ���
A����ʯ�� B����ʯ�� C������������ D���ռ�
��2��Bװ�õ����� ��Eװ�õ����� ��
��3��ͨ��Cװ�õ�����������߽ϳ����ұ߽϶̣�Ŀ����  ��
��
��4��װ��F�з�����Ӧ�Ļ�ѧ����ʽ�� ��
��5��װ��C�ڳ���Ũ��İ��̲��������ڱ����ᣬ��һ�������ǿ�������Ҫ�ɷ�֮һ����д����Ӧ�Ļ�ѧ����ʽ�� ������a mol�����μӷ�Ӧʱ��ת�Ƶĵ�������Ϊb�������ӵ���������Ϊ mol-1 ���ú�a��b�Ĵ���ʽ��ʾ����
��6����װ��C��G���ݳ���β���п��ܺ��л���ɫ���ж����壬��δ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�츣��ʡ������ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ᴿ�������ʣ�����������Ϊ���ʣ���ʵ�������������
A����������Һ��������������ͨ��������������ַ�Ӧ����ȣ�ʹ���������ݳ�
B��ʳ�Σ�NH4Cl�����ӹ����ռ��������
C��SO2��SO3����ͨ��ʢ��Ũ�����ϴ��ƿ
D��������壨С�մ������������������м���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�츣��ʡ������ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Լ�����������ɫ�����������Լ�ƿ�����
A������ B������ C����ˮ D������������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ɽ��ʡ��һ12���¿���ѧ�Ծ��������棩 ���ͣ������
2.3g Na�ڸ���Ŀ����г�ʱ����ã��õ�Na��������3.5g��ȷ��������������Ϊ_____________�����ǵ������ֱ�Ϊ_____________������������Ͷ������ˮ�У��ɵ�O2__________g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�˴��и߶����¿�����ѧ���������棩 ���ͣ������
��1����֪����298K��101kPaʱ��
��C(s,ʯī)��O2(g) = CO2(g) ��H1 = ��400 kJ��mol��1��
��2H2(g)��O2(g) = 2H2O(l) ��H2 = ��570 kJ��mol��1��
��2C2H2(g)��5O2(g) = 4CO2(g)+ 2H2O(l) ��H3 = ��2600 kJ��mol��1��
д��298Kʱ��C(s,ʯī)��H2(g)����1 mol C2H2(g)��Ӧ���Ȼ�ѧ����ʽ ��������Ϊ�������Һ�����ݷ�Ӧ�����һ��ȼ�ϵ�أ�д����缫��Ӧʽ ��
��2����ҵ�ϳɰ��ķ�Ӧԭ��Ϊ N2(g)+3H2(g) 2NH3(g) ��H=-92.4 kJ��mol-1ij�¶��£���10 mol N2��
2NH3(g) ��H=-92.4 kJ��mol-1ij�¶��£���10 mol N2�� 25mol H2�����ݻ�Ϊ10 L���ܱ������ڣ�10 minʱ��Ӧ�ﵽƽ��״̬����õ�����ƽ��ת����Ϊ50%����10 min�ڸ÷�Ӧ��ƽ������v(H2)= mol��L-1��min-1������¶��¸÷�Ӧ��ƽ�ⳣ��K= ��
25mol H2�����ݻ�Ϊ10 L���ܱ������ڣ�10 minʱ��Ӧ�ﵽƽ��״̬����õ�����ƽ��ת����Ϊ50%����10 min�ڸ÷�Ӧ��ƽ������v(H2)= mol��L-1��min-1������¶��¸÷�Ӧ��ƽ�ⳣ��K= ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com