
 )的过程中,欲使原子利用率达到最高,还需要其他的反应物是( )
)的过程中,欲使原子利用率达到最高,还需要其他的反应物是( )| A. | CO和CH3OH | B. | CO2和H2O | C. | H2和CO2 | D. | CH3OH和H2 |
分析 由题意知,绿色化学即环境友好型化学,其理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%,根据这一观点,要把一个C3H4分子变成一个甲基丙烯酸甲酯C5H8O2分子,还必须增加2个C原子、4个H原子、2个O原子,即原料中C、H、O的原子个数比为2:4:2,以此来解答.
解答 解:由题意知,绿色化学即环境友好型化学,其理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%,根据这一观点,要把一个C3H4分子变成一个甲基丙烯酸甲酯C5H8O2分子,还必须增加2个C原子、4个H原子、2个O原子,即原料中C、H、O的原子个数比为2:4:2.
A.CH3OH和CO,这两种物质如果按照分子个数比1:1组合,则很容易使C、H、O的原子个数比达到2:4:2,故A正确;
B.C02和H2O,其中两种物质里三种原子不论怎样组合也都不能使C、H、O的原子个数比为2:4:2,故B错误;
C.CO2和H2,两种物质分子里三种原子不论怎样组合也都不能使C、H、O的原子个数比为2:4:2,故C错误;
D.CH3OH和H2,其中两种物质分子里三种原子不论怎样组合都不能使C、H、O的原子个数比为2:4:2,故D错误;
故选A.
点评 本题考查绿色化学的概念,为高频考点,侧重于学生的分析能力和计算能力的考查,并以此为依据,考查元素种类、原子种类在化学变化中都保持不变,因此我们要用守恒的观点来解答,注意解本题时一定要读懂题意,明确命题者的意图,再结合所学方可解答,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 1mol苯乙烯(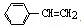 )中含有的C=C数为4NA )中含有的C=C数为4NA | |
| B. | 标准状况下,2.24L己烷含有的分子数为0.1NA | |
| C. | 1mol甲基含10NA个电子 | |
| D. | 某温度下,2.6g乙炔和苯的混合气体中所含碳原子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
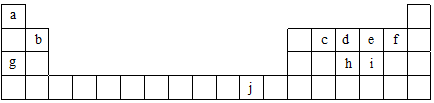
 .
. ,ci2与ce2比较,沸点较高的是CS2(写分子式).
,ci2与ce2比较,沸点较高的是CS2(写分子式).查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,名称是:3-甲基-1-丁炔.
,名称是:3-甲基-1-丁炔.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 用中和滴定法测定某盐酸的物质的量浓度.
用中和滴定法测定某盐酸的物质的量浓度.| 滴定次数 | 待测液体体积/mL | 标准碱液 | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| ① | 20.0 | 0.40 | 20.41 |
| ② | 20.0 | 0.10 | 20.60 |
| ③ | 20.0 | 4.00 | 23.99 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
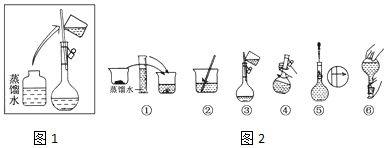
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 可将地下钢管与外加直流电源的负极相连以保护它不受腐蚀 | |
| C. | “静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量 | |
| D. | 电解MgCl2溶液,可制得金属镁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com