
| A. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| B. | 标准状况下,2.24 L CCl4含有的共价键数为0.4NA | |
| C. | 14 g乙烯和丙烯混合气体中的氢原子数为2NA | |
| D. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA |
分析 A.D2O和H2O摩尔质量不同,含有质子数相同1个分子都含有10个质子;
B.标况下四氯化碳为液体;
C.乙烯和丙烯的最简式均为CH2;
D.过氧化钠和水的反应中,氧元素的价态由-1价变为0价.
解答 解:A.D2O和H2O摩尔质量不同,则相同质量的二者依据n=$\frac{m}{M}$可知,水分子物质的量不同,所以含有质子数不同,故A错误;
B.标况下四氯化碳为液体,不能使用气体摩尔体积,故B错误;
C.乙烯和丙烯的最简式均为CH2,故14g混合物中含1molCH2,故含2NA个氢原子,故C正确;
D.过氧化钠和水的反应中,氧元素的价态由-1价变为0价,故当生成0.1mol氧气时,转移0.2NA个电子,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是物质组成、氧化还原反应电子转移数目计算、气体摩尔体积等知识点的应用,掌握基础是解题关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 氨分子中氮的化合价为-3价 | |
| B. | 氨在常温下是一种气体 | |
| C. | 氨易液化,液氨气化时吸收大量的热 | |
| D. | 氨极易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
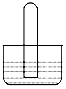
| A. | 若水槽中是NaOH溶液,试管中是CO2,可看到试管中液面上升很少 | |
| B. | 若水槽中是水,试管中是NO2,可看到液面上升并充满整个试管 | |
| C. | 若水槽中是水并滴有几滴酚酞,试管中是NH3,可看到试管中液体上升并呈红色 | |
| D. | 若水槽中是水并滴有几滴紫色石蕊,试管中是SO2,可看到液面上升并褪为无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②④ | B. | 只有①③ | C. | 只有②③ | D. | 只有①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15g-CH3含有的电子数目为7 NA | |
| B. | 1 mol Fe的粉末与足量浓硫酸加热反应,转移电子的数目为2 NA | |
| C. | 室温,28 g由C3H6和C4H8组成的混合物中含有氢原子的数目为4 NA | |
| D. | 标准状况下,22.4 L 1,2-二溴乙烷的分子数约为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①②④⑥ | C. | ⑤⑥⑦ | D. | ②③⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 滴定次数 | 待测液的体积(mL) | 滴定前的读数(mL) | 滴定后的读数(mL) |
| 第一次 | 25.00 | 0.00 | 15.90 |
| 第二次 | 25.00 | 0.00 | 14.99 |
| 第三次 | 25.00 | 0.00 | 15.01 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com