
【题目】化学与人类生活、社会可持续发展密切相关,下列说法正确的是
A.地球上最基本的能源是化学能
B.太阳能热水器、沼气的使用、玉米制乙醇都涉及生物质能的利用
C.利用二氧化碳制造全降解塑料能有效减少“白色污染”
D.人们可以把放热反应释放的能量转化为其它可利用的能量,而吸热反应没有利用价值
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】计算并按要求填空。
(1)已知16g CH4(g)与适量O2(g)反应生成CO2(g)和H2O(l)放出890.3kJ热量,写出该反应对应的热化学方程式___________________________________;
(2)已知1g C2H2完全燃烧生成CO2(g)和H2O(l)放出的热量为50.0kJ,写出表示C2H2标准燃烧热的热化学方程式_________________________________________;
(3)已知拆开1mol H-H键,1mol N-H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为________________;
(4)某种优质燃油由甲、乙两种有机物混合而成,甲、乙两种物质含有C、H、O三种元素中的两种或三种。已知甲、乙及CO、H2的燃烧热如下:
物质 | 甲 | 乙 | CO | H2 |
燃烧热/kJmol-1 | 1366 | 5518 | 283 | 286 |
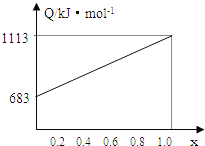
取甲、乙按不同比例混合的燃油23g,在足量的O2中燃烧时,放出的热量Q与混合物中乙的物质的量分数x的关系如图。试求:
(a)乙的相对分子质量为____________;
(b)1mol由甲、乙等物质的量混合而成的燃油在一定量的O2中燃烧,放出热量2876kJmol-1,则反应中生成CO__________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,已知:A位于第3周期ⅦA族;B是形成化合物种类最多的元素;C2-离子与氩原子具有相同的电子层结构;D原子结构示意图为: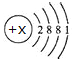 。
。
试写出:
(1)A元素的符号是_____,B元素在周期表中的位置______________________。
(2)B的最高价氧化物的电子式为___________________________;
C2-离子的电子式_____________________D的原子序数为_________。
(3)A、D分别对应的最高价氧化物水化物之间反应的离子方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,已知A元素最低化合价为-3价,它的最高价氧化物含氧56.36%,原子核内中子数比质子数多1个,试回答:
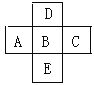
⑴写出它们的元素符号:
A________B________C________D________E_________。
⑵A、B、C、D的气态氢化物稳定性最差的是_______。
⑶A、B、C的原子半径由小到大的顺序是_________。
⑷A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X的结构是![]() (其中I、II为未知部分的结构)。下列是X发生反应的转化关系图及E的信息。
(其中I、II为未知部分的结构)。下列是X发生反应的转化关系图及E的信息。

E的组成或结构信息
①分子中含18O及苯环结构
②核磁共振氢谱有4个峰,峰面积之比是1:1:2:2
③与NaHCO3溶液反应产生CO2
请回答:
(1)有机物E中含有的官能团名称是_______________,G的名称是_______________,X与氢氧化钠的反应类型为_______________。
(2)B与G反应可生成高分子化合物M,其化学方程式是_______________。
(3)X的结构简式是_______________。
(4)A中通入过量二氧化碳的化学方程式为_________________________________________。
(5)已知E的同系物H的相对分子质量比E多14。H的同分异构体中,能同时满足下列条件的共有___________种(不考虑立体异构)。
①能发生银镜反应;②能发生水解反应;③能与FeCl3溶液发生显色反应。
其中核磁共振氢谱为5组峰,且峰面积比为1∶1∶2∶2∶2的为_________(写结构简式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ti、Fe、Cr、Mn等均为过渡元素,在生产生活中起着不可替代的重要作用,对其单质和化合物的应用研究是目前科学研究的前沿之一。请回答下列问题:
(1)Cr元素的基态原子电子排布式为_____________________,比较Fe和Mn的各级电离能后发现,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子______(填“难”或“易”)。
(2)Cu元素处于周期表____________区,向盛有硫酸铜的试管里加入氨水,首先形成蓝色沉淀,继续加入氨水,沉淀溶解,此时的离子方程式为______________,若加入乙醇将析出____________色的晶体,其配离子的离子构型为_____________
(3)某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应(巨磁电阻效应)。用A、B、O表示这类特殊晶体的化学式:_____________。
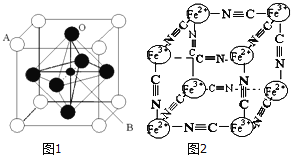
(4)有一种蓝色晶体可表示为:[KxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上,K+位于上述晶胞体心,且K+空缺率为50%(体心中没有K+的占总体心的百分比),其晶体中的阴离子晶胞结构如上图的图2所示,该晶体的化学式可表示为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①氯化钠溶液和鸡蛋清 ②氯化钠溶液中少量的硝酸钾 ③碳酸钡和氯化钡的溶液分离以上三组混合物依次采取的方法正确的是( )
A .渗析、结晶、过滤 B.渗析、蒸馏、过滤
C .蒸馏、萃取、分液 D.分液、过滤、加热升华
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃分子的球棍模型,据此回答下列问题:
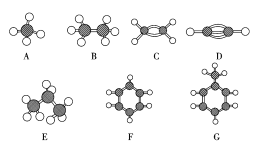
(1)书写结构简式:C____________F_____________
(2)能够发生加成反应的烃有________(填数字)种。
(3)一卤代物种类最多的是________(填对应字母)。
(4)等质量的上述六种烃,完全燃烧时消耗O2最多的是________(填对应字母)。等物质的量的上述六种烃,完全燃烧时消耗O2最多的是________(填对应字母)。
(5)在120 ℃,1.01×105 Pa下与足量O2混合点燃,完全燃烧后气体体积没有变化的烃是________(填对应字母)。
(6)常温下含碳量最高的烃是________(填对应字母)。
(7)写出F发生溴代反应的化学方程式_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在科学研究和工业生产中具有许多用途。请回答下列问题:
(1)画出基态Cu原子的价电子排布图_______________;
(2)已知高温下Cu2O比CuO稳定,从核外电子排布角度解释高温下Cu2O更稳定的原因____________________________________;
(3)配合物[Cu(NH3)2]OOCCH3中碳原子的杂化类型是___________,配体中提供孤对电子的原子是________。C、N、O三元素的第一电离能由大到小的顺序是_______________(用元素符号表示)。
(4)铜晶体中铜原子的堆积方式如图1所示,则晶体铜原子的堆积方式为____________。
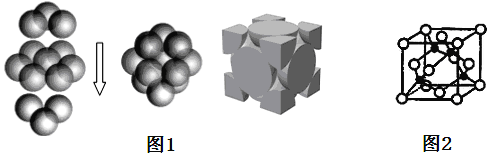
(5)M原子的价电子排布式为3s23p5,铜与M形成化合物的晶胞如图2所示(黑点代表铜原子)。
①该晶体的化学式为_____________。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于________化合物(填“离子”、“共价”)。
③已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,已知该晶体中Cu原子和M原子之间的最短距离为体对角线的1/4,则该晶体中Cu原子和M原子之间的最短距离为___________pm(写出计算列式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com