
【题目】在xR++yH++O2=mR2++nH2O离子方程式中,m值是
A.2x B.4 C.4 D.2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图为周期表的一小部分,A、B、C、D的位置关系如图所示。且它们均为短周期元素,其中C元素的最外层电子数是电子层数的2倍,回答下列问题:

(1)在B、C、D最高价氧化物对应水化物中,B的化学式为______,其中酸性最强的是_____。
(2)在A、B、C、所形成氢化物中,A的化学式:___________,其中最稳定的是___________。
(3)写D的单质与C的氢化物反应的化学方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按系统命名法命名:
①(CH3)2CH(CH2)2CH(C2H5) (CH2)2(CH3)的名称:_________________。
② 的名称:________________。
的名称:________________。
(2)溴乙烷发生消去反应的化学方程式:____________________________。
(3)乙醛发生银镜反应的化学方程式:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫的化合物种类较多,用途广泛。
I:焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一,其制备的反应原理为:Na2SO3+ SO2==Na2S2O5
某研究小组利用下图装置制取Na2S2O5,盛硫酸的仪器叫分液漏斗。

(1)写出装置甲中发生反应的化学方程式__________________。
(2)关闭K3,要求只检查装置甲的气密性,请至少写出两种不同的操作方法。
方法1:_________________________。
方法2:_________________________。
方法3:_________________________。
(3)装置乙的作用是________________。
(4)写出焦亚硫酸钠晶体在空气中被完全氧化的化学方程式_____________。
II:硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3 、FeCl2、CuCl2的混合溶液中反应用以回收S,其物质转化如图所示。

(1)反应中当有34gH2S转化为硫单质时,保持溶液中Fe3+的量不变,需要消耗O2的质量为 _____________。
(2)在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施是___________________。
(3)写出图中各步转化的化学方程式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当Mg(OH)2在水中达到溶解平衡时:Mg(OH)2(s)Mg2+(aq)+2OH﹣(aq)要使Mg(OH)2进一步溶解,应向溶液中加少量的固体是
A.NH4Cl B.NaOH C.Na2CO3 D.Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸的过程中,SO2催化氧化的原理为:2SO2(g) + O2(g) ![]() 2SO3(g) + Q
2SO3(g) + Q ![]()
(1)若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减小”或“不变”)
|
| 平衡常数K |
________ | ________ | ________ |
(2)2SO2(g) + O2(g) ![]() 2SO3(g)过程的能量变化如图所示。下列说法正确的是_________
2SO3(g)过程的能量变化如图所示。下列说法正确的是_________
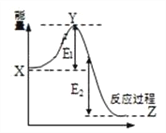
A.加入催化剂,X点位置升高
B.反应热 = E1 + E2
C.反应物总能量低于生成物
D.加入催化剂,E2不变
(3)将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应得到如下表中的两组数据:
实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | ||
SO2 | O2 | SO2 | O2 | ||
1 | T1 | 4 | 2 | x | 0.8 |
2 | T2 | 4 | 2 | 0.4 | y |
实验1从开始到反应达到化学平衡时,用去时间2分钟,则υ(SO2)表示的反应速率为_________;T1________T2(填“>”、“<”或“=”)。制取SO2的尾气用NaOH溶液吸收,可得到Na2SO3和NaHSO3两种盐。
(4)0.1mol/L的NaHSO3溶液中c(H+) > c(OH-),用水解和电离理论的角度解释其原因___________________;若往溶液中加入氨水至中性,则c(Na+)______c(HSO3-) + c(SO32-) + c(H2SO3)(填“>”、“﹤”或“=”)。
(5)往0.1 mol/L的Na2SO3溶液加入少量Na2SO3固体,完全溶解后溶液中c(Na+) : c(SO32-)的比值____________(填“变大”、“变小”或“保持不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出制取硝基苯的化学反应方程式_________________________________;
(2)写出镁铝氢氧化钠原电池的负极电极反应式___________________________;
(3)氯气是重要的化工原料,可以用来制备很多化工产品,比如可以制备净水剂高铁酸钾(K2FeO4),写出碱性条件下,由氯化铁制备高铁酸钾的离子方程式___________;
写出工业制漂白粉的化学反应方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有HCO3﹣、Na+、Ba2+、NO3﹣4种离子,若向其中加入少量Na2O2固体后溶液中离子浓度基本保持不变的是( )
A.HCO3﹣
B.Na+
C.Ba2+
D.NO3﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com