
醛或酮与氰化钠、氯化铵反应,生成氨基腈,经水解生成氨基酸盐,是制备氨基酸盐的一种简便方法,反应过程如下:

下列有关该反应说法不合理的是( )
A.反应①是加成反应
B.反应②需要在酸性环境中进行
C.反应②为碱性环境时,产物结构简式是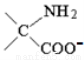
D.经过上述反应,苯乙醛可以制得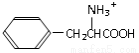
科目:高中化学 来源:2016届湖北省沙市高三高考前最后一卷理综化学试卷(解析版) 题型:填空题
由Ca3(PO4)2 、SiO2 、焦炭等为原料生产硅胶(SiO2·nH2O)、磷、磷酸及CH3OH,下列工艺过程原料综合利用率高,废弃物少。
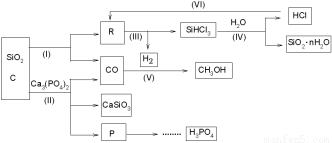
(1)上述反应中,属于置换反应的是 [选填:(Ⅰ)、(Ⅱ)、(Ⅲ)、(Ⅳ)、(Ⅴ)]。
(2)高温下进行的反应Ⅱ的化学方程式为 ;固体废弃物CaSiO3可用于 。(答一条即可)
(3)反应Ⅲ需在隔绝氧气和无水条件下进行,其原因是 。
(4)CH3OH可用作燃料电池的燃料,在强酸性介质中,负极的电极反应式为 。
(5)指出(VI)这一环节在工业生产上的意义 。
(6)写出由P→H3PO4 的有关反应式:
① 。 ② 。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省等三校高三第四次模拟化学试卷(解析版) 题型:选择题
下列化学反应的离子方程式正确的是
A.Ba(OH)2溶液中滴加NH4HSO4溶液至Ba2+沉淀完全:Ba2++OH-+H++SO42-=BaSO4↓+H2O
B.将过量SO2气体通入氨水中:SO2 + NH3·H2O =NH4++ HSO3-
C.用醋酸除去水垢中的CaCO3 : CaCO3 + 2 H+=Ca2++ H2O+CO2↑
D.用KIO3氧化酸性溶液中的KI: 5I-+IO3- +3H2O=3I2+6OH-
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三5月模拟四理综化学试卷(解析版) 题型:选择题
下图是一种蓄电池的示意图。被膜隔开的电解质分别为Na2S2和NaBr3,放电后变为Na2S4和NaBr。已知放电时Na+ 由乙池向甲池移动。下面对该装置工作过程中叙述正确的是
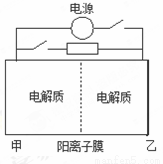
A.放电过程,甲池发生氧化反应
B.放电过程,电池反应:2S22-+ Br3-= S42-+ 3Br-
C.充电过程,乙池为阳极室
D.充电过程,当阳极室阴离子增加2mol,整个电路中电子转移2mol
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三5月模拟三理综化学试卷(解析版) 题型:实验题
为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:
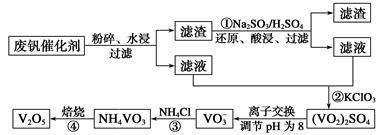
部分含钒物质在水中的溶解性如下:
物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
回答下列问题:
(1)工业由V2O5冶炼金属钒常用铝热剂法,写出该反应的化学方程式 .
(2)图中所示滤液中含钒的主要成分为 (写化学式).
有学者建议将滤液进行如下处理后再用KClO3氧化
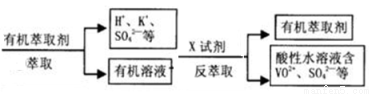
上图中的萃取与反萃取的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂).
RSO4(水层)+ 2HA(有机层) RA2(有机层)+H2SO4(水层),上图中的X试剂为 _____;这种萃取与反萃取过程有别于用CCl4萃取碘水中的碘,二者的相同点是__________________,不同点是_______________
RA2(有机层)+H2SO4(水层),上图中的X试剂为 _____;这种萃取与反萃取过程有别于用CCl4萃取碘水中的碘,二者的相同点是__________________,不同点是_______________
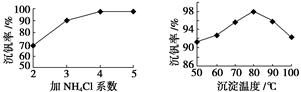
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式_____________ ;沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度.根据下图判断最佳控制氯化铵系数和温度为 、 .
(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,完成反应的离子方程式为□VO2++□H2C2O4+□_____=□VO2++□CO2↑+□H2O.
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为:
VO2++V2++2H+  VO2++H2O+V3+
VO2++H2O+V3+
电池充电时阳极的电极反应式为__________________.
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三下学期猜题理综化学试卷(解析版) 题型:填空题
太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置。其材料有单晶硅,还有铜、锗、镓、硒等化合物。
(1)基态亚铜离子中电子占据的原子轨道数目为____________。
(2)若基态硒原子价层电子排布式写成4s24px24py4,则其违背了____________。
(3)左下图表示碳、硅和磷元素的四级电离能变化趋势,其中表示磷的曲线是____________(填标号)。
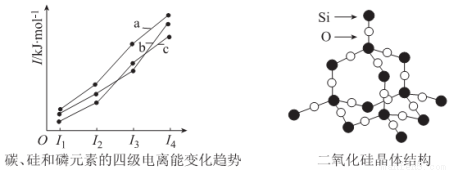
(4)单晶硅可由二氧化硅制得,二氧化硅晶体结构如右上图所示,在二氧化硅晶体中,Si、O
原子所连接的最小环为____________元环,则每个O原子连接____________个最小环。
(5)与镓元素处于同一主族的硼元素具有缺电子性。自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作Na2B4O7·10H2O,实际上它的结构单元是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,应该写成Na2[B4O5(OH)4]8H2O.其结构如图所示,它的阴离子可形成链状结构。
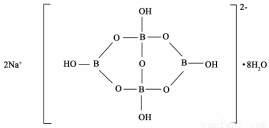
①该晶体中不存在的作用力是____________(填选项字母)。
A.离子键B.共价键C.金属键D.范德华力E.氢键
②阴离子通过____________相互结合形成链状结构。
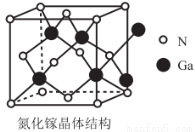
(6)氮化嫁(GaN)的晶体结构如图所示。晶体中N、Ga原子的轨道杂化类型是否相同____________(填“是”或“否”),判断该晶体结构中存在配位键的依据是____________。

(7)某光电材料由锗的氧化物与铜的氧化物按一定比例熔合而成,其中锗的氧化物晶胞结构如下图所示,该物质的化学式为____________。已知该晶体密度为7.4g/cm3,晶胞边长为4.3×10-10m。则锗的相对原子质量为____________(保留小数点后一位)。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三下学期猜题理综化学试卷(解析版) 题型:选择题
分子式为C5H9O4N,只含有羧基和氨基两种官能团的同分异构体共有
A.8种 B.9种 C.10种 D.11种
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三高考打靶测试理综化学试卷(解析版) 题型:选择题
从安全的角度,下列说法正确的是
A.水银温度计不慎打破,用胶头滴管将水银吸出放入水封的瓶中,残破的温度计插入装有硫粉的广口瓶中
B.用氢气还原氧化铜的实验中,开始应该先点燃酒精灯后通氢气
C.遇到氯气泄漏时,应立即关闭氯气罐,用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处
D.乘坐火车时,严禁携带白磷、汽油、氯化钠等易燃易爆物品
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前模拟理综化学试卷(解析版) 题型:选择题
已知戊烷有3种同分异构体,戊基有8种同分异构体,则戊醇的同分异构体(属醇类)的数目有 ( )
A.5 种 B.6 种 C.7 种 D.8 种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com