
”¾ĢāÄæ”æŠĀÄÜŌ“Ęū³µµÄŗĖŠÄ²æ¼žŹĒļ®Ąė×Óµē³Ų£¬³£ÓĆĮ×ĖįŃĒĢśļ®(LiFePO4)×öµē¼«²ÄĮĻ”£¶ŌLiFePO4·Ļ¾Éµē¼«£Øŗ¬ŌÓÖŹAl”¢ŹÆÄ«·Ū£©»ŲŹÕ²¢»ńµĆøß“æLi2CO3µÄ¹¤ŅµĮ÷³ĢČēĶ¼£ŗ
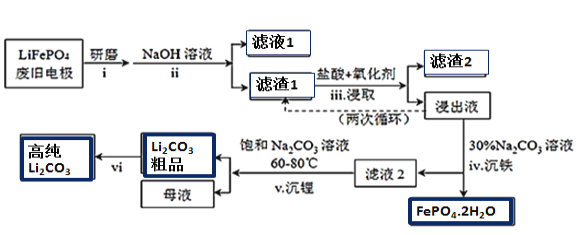
׏ĮĻ£ŗĢ¼Ėįļ®ŌŚĖ®ÖŠČܽā¶ČĖęĪĀ¶Č±ä»ÆČēĻĀ£ŗ
ĪĀ¶Č/”ę | 0 | 20 | 40 | 60 | 80 | 100 |
Čܽā¶Č/g | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(1)¹ż³ĢiŃŠÄ„·ŪĖéµÄÄæµÄŹĒ__________________”£
(2)¹ż³Ģii¼ÓČė×ćĮæNaOHČÜŅŗµÄ×÷ÓĆ(ÓĆ»Æѧ·“Ó¦·½³ĢŹ½±ķŹ¾)_________________”£
(3)Čē¹ż³Ģiii²ÉÓĆNaClO3×÷ĪŖŃõ»Æ¼Į£¬Ōņ¹ż³ĢÖŠ»į·“Ó¦»į·¢Éśø±·“Ӧɜ³É»ĘĀĢÉ«ĘųĢ壬
¢ŁøĆø±·“Ó¦¶ŌÓ¦µÄĄė×Ó·½³ĢŹ½ĪŖ_______________________________________________________£»
“Ó»·±£½Ē¶Č·ÖĪö£¬Ń”Ōń___________(Ģī×ÖÄø)×÷ĪŖøĆ¹ż³ĢµÄŃõ»Æ¼Į»įøüŗĆ”£
a.H2O2 b.ÅØĮņĖį c.ÅØHNO3
¢Ś¹ż³ĢiiiµĆµ½µÄ½ž³öŅŗŃ»·Į½“ĪµÄÄæµÄŹĒ________________________________________________”£
(4)½ž³öŅŗÖŠ“ęŌŚ“óĮæH2PO4©ŗĶHPO42-£¬ŅŃÖŖ£ŗ![]() £¬½įŗĻĘ½ŗāŅʶÆŌĄķ£¬½āŹĶ¹ż³ĢivµĆµ½Į×ĖįĢś¾§ĢåµÄŌŅņ______________________________________”£
£¬½įŗĻĘ½ŗāŅʶÆŌĄķ£¬½āŹĶ¹ż³ĢivµĆµ½Į×ĖįĢś¾§ĢåµÄŌŅņ______________________________________”£
(5)¼ņŹö¹ż³ĢviµÄ²Ł×÷______________________________________________________________”£
”¾“š°ø”æŌö“ó½Ó“„Ć껿£¬¼Óæģ·“Ó¦ĖŁĀŹ 2Al + 2NaOH + 2H2O=2NaAlO2+3H2”ü ClO3- +5Cl- + 6H+ = 3Cl2”ü+ 3H2O A ĢįøßŃõ»Æ¼ĮŗĶĖįµÄĄūÓĆĀŹ£Ø»ņĢįøß½ž³öŅŗÖŠLi+ÅØ¶Č£¬½ŚŌ¼ŗóŠų“æ¼īµÄÓĆĮ棩 CO32©½įŗĻH+£¬c(H+)¼õŠ”£¬ÉĻŹöĮ½øöµēĄėĘ½ŗā¾łĻņÓŅŅĘ¶Æ£¬c(PO43©)Ōö“ó£¬ÓėFe3+½įŗĻŠĪ³ÉĮ×ĖįĢś¾§Ģå ÓĆČČĖ®Ļ“µÓ”¢øÉŌļ
”¾½āĪö”æ
£Ø1£©øł¾ŻÓ°Ļģ·“Ó¦ĖŁĀŹµÄŅņĖŲ·ÖĪö¹ż³ĢiŃŠÄ„·ŪĖéµÄÄæµÄ£»
£Ø2£©øł¾ŻĀĮæÉŅŌČÜÓŚĒāŃõ»ÆÄĘČÜŅŗ·ÖĪö£»
£Ø3£©¢Ł¹ż³ĢiiiÖŠNaClO3»įÓėŃĪĖį·¢Éś·“Ӧɜ³ÉĀČĘų”¢ĀČ»ÆÄĘ”¢Ė®£»“Ó»·±£½Ē¶Č·ÖĪöŃ”Ōń¶Ō»·¾³ĪŽĪŪČ¾µÄĪļÖŹ×öŃõ»Æ¼ĮøüŗĆ£»
¢Ś½ž³öŅŗŃ»·ĄūÓĆæÉŅŌĢįøßŃõ»Æ¼ĮŗĶĖįµÄĄūÓĆĀŹ£¬Ģįøß½ž³öŅŗÖŠLi+ÅØ¶Č£¬½ŚŌ¼ŗóŠų“æ¼īµÄÓĆĮ棻
£Ø4£©¹ż³Ģiv¼ÓČėĢ¼ĖįÄĘČÜŅŗæÉŅŌĢįøßc(PO43©)£¬“Ó¶ųŹµĻÖ³ĮĢś£»
£Ø5£©øł¾ŻĪĀ¶ČŌ½øßĢ¼Ėįļ®Čܽā¶ČŌ½Š”·ÖĪö”£
£Ø1£© ¹ż³ĢiŃŠÄ„·ŪĖéµÄÄæµÄŹĒŌö“ó½Ó“„Ć껿£¬¼Óæģ·“Ó¦ĖŁĀŹ£»
¹Ź“š°øĪŖ£ŗŌö“ó½Ó“„Ć껿£¬¼Óæģ·“Ó¦ĖŁĀŹ£»
£Ø2£© ĀĮæÉŅŌČÜÓŚĒāŃõ»ÆÄĘČÜŅŗÉś³ÉĘ«ĀĮĖįÄĘ£¬ĖłŅŌ¹ż³Ģii¼ÓČė×ćĮæNaOHČÜŅŗµÄ×÷ÓĆŹĒČܽāĀĮ£¬Ź¹Ęä·ÖĄė³öČ„£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2Al + 2NaOH + 2H2O=2NaAlO2+3H2”ü£»
¹Ź“š°øĪŖ£ŗ2Al + 2NaOH + 2H2O=2NaAlO2+3H2”ü£»
£Ø3£© ¢Ł¹ż³ĢiiiÖŠNaClO3»įÓėŃĪĖį·¢Éś·“Ӧɜ³ÉĀČĘų”¢ĀČ»ÆÄĘ”¢Ė®£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ
ClO3- +5Cl- + 6H+ = 3Cl2”ü+ 3H2O£»¹ż³ĢiiiČōÓĆH2O2×öŃõ»Æ¼Į£¬²śĪļŹĒH2O£¬ĪŽĪŪČ¾£¬ÅØĮņĖį”¢ÅØHNO3×÷ĪŖŃõ»Æ¼Į£¬²śĪļ·Ö±šĪŖ¶žŃõ»ÆĮņ”¢µŖŃõ»ÆĪļ£¬ĪŪČ¾»·¾³£¬ĖłŅŌ“Ó»·±£½Ē¶Č·ÖĪöŃ”ŌńH2O2×÷ĪŖøĆ¹ż³ĢµÄŃõ»Æ¼Į»įøüŗĆ£»
¹Ź“š°øĪŖ£ŗClO3- +5Cl- + 6H+ = 3Cl2”ü+ 3H2O£»H2O2 £»
¢Ś¹ż³ĢiiiµĆµ½µÄ½ž³öŅŗŃ»·Į½“ĪµÄÄæµÄŹĒĢįøßŃõ»Æ¼ĮŗĶĖįµÄĄūÓĆĀŹ£¬Ģįøß½ž³öŅŗÖŠLi+ÅØ¶Č£¬½ŚŌ¼ŗóŠų“æ¼īµÄÓĆĮ棻
¹Ź“š°øĪŖ£ŗĢįøßŃõ»Æ¼ĮŗĶĖįµÄĄūÓĆĀŹ£¬Ģįøß½ž³öŅŗÖŠLi+ÅØ¶Č£¬½ŚŌ¼ŗóŠų“æ¼īµÄÓĆĮ棻
£Ø4£© ¹ż³Ģiv¼ÓČėĢ¼ĖįÄĘČÜŅŗæÉŅŌĢįøßc(PO43©)£¬CO32©½įŗĻH+£¬c(H+)¼õŠ”£¬ÉĻŹöĮ½øöµēĄėĘ½ŗā¾łĻņÓŅŅĘ¶Æ£¬c(PO43©)Ōö“ó£¬ÓėFe3+½įŗĻŠĪ³ÉĮ×ĖįĢś¾§Ģ壻
¹Ź“š°øĪŖ£ŗCO32©½įŗĻH+£¬c(H+)¼õŠ”£¬ÉĻŹöĮ½øöµēĄėĘ½ŗā¾łĻņÓŅŅĘ¶Æ£¬c(PO43©)Ōö“ó£¬ÓėFe3+½įŗĻŠĪ³ÉĮ×ĖįĢś¾§Ģ壻
£Ø5£© ĪĀ¶ČŌ½øßĢ¼Ėįļ®Čܽā¶ČŌ½Š”£¬Ņņ“Ė¹ż³ĢviµÄ²Ł×÷ŹĒÓĆČČĖ®Ļ“µÓ”¢øÉŌļ£»
¹Ź“š°øĪŖ£ŗÓĆČČĖ®Ļ“µÓ”¢øÉŌļ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±¾ĢāĪŖŃ”×öĢā£¬°üĄØA”¢BĮ½Ģā”£Ń”ѧ”¶»ÆѧÓėÉś»ī”·Ä£æéµÄæ¼Éś“šAĢā£¬Ń”ѧ”¶ÓŠ»ś»Æѧ»ł“””·Ä£æéµÄæ¼Éś“šBĢā£¬ĆæĪ»æ¼ÉśÖ»æÉŃ”×ölĢā”£ČōĮ½Ģā¶¼×÷“š£¬ŌņŅŌAĢā¼Ę·Ö”£
A”¶»ÆѧÓėÉś»ī”·
(1)·ĄÖĪ»·¾³ĪŪČ¾”¢øÄÉĘÉśĢ¬»·¾³ŅŃ³ÉĪŖČ«ČĖĄąµÄ¹²Ź¶”£
¢ŁĻĀĮŠø÷ĻīÖŠ£¬Ķź³ÉæÕĘųÖŹĮæ±Øøꏱ²»ŠčŅŖ¼ą²āµÄŹĒ______(Ģī×ÖÄø)”£
a£®¶žŃõ»ÆĢ¼µÄÅØ¶Č b£®¶žŃõ»ÆĮņµÄÅØ¶Č c£®æÉĪüČėæÅĮ£ĪļµÄÅضČ
¢ŚĻĀĮŠ×ö·ØÖŠ²»ĄūÓŚøÄÉĘ»·¾³ÖŹĮæµÄŹĒ______(Ģī×ÖÄø)”£
a£®½«·Ļ¾Éµē³Ų½ųŠŠÉīĀń“¦Ąķ
b£®³ä·ÖĄūÓĆ·ēÄܵȊĀÄÜŌ“
c£®øųĘū³µ¼Ó×°Ī²Ęų“߻ƾ»»Æ×°ÖĆ
¢Ū¹¤Ņµ·ĻĖ®Šč“¦Ąķ“ļ±źŗó²ÅÄÜÅÅ·Å”£ŌžøÖ³§ÅųöµÄ·ĻĖ®Ö÷ŅŖŹĒŗ¬ŃĪĖįµÄĖįŠŌ·ĻĖ®£¬“¦Ąķ“Ė·ĻĖ®æɲÉÓƵķ½·ØŹĒ______(Ģī×ÖÄø)”£
a£®Ńõ»Æ»¹Ō·Ø b£®ÖŠŗĶ·Ø c£®³Įµķ·Ø
¢ÜĆŗĢæÖ±½ÓČ¼ÉÕŅżĘš¶ąÖÖ»·¾³ĪŹĢā”£Č¼Ćŗ²śÉśµÄSO2Ōö¼ÓĮĖ______ŠĪ³ÉµÄæÉÄÜ£»“¦Ąķŗ¬CO”¢SO2ŃĢµĄĘųĪŪČ¾µÄŅ»ÖÖ·½·ØŹĒ½«ĘäŌŚ“߻ƼĮ×÷ÓĆĻĀ×Ŗ»ÆĪŖµ„ÖŹS£¬·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____________________”£
(2)ŗĻĄķÓ¦ÓĆ»ÆѧÖŖŹ¶æÉŅŌøüŗƵŲČĻŹ¶Éś»ī”¢øÄÉĘÉś»ī”£
¢ŁµČÖŹĮæµÄĢĒĄą”¢ÓĶÖ¬”¢µ°°×ÖŹÖŠ£¬Ģį¹©ÄÜĮæ×ī¶ąµÄŹĒ______”£µ°°×ÖŹĖ®½āæÉŅŌµĆµ½______”£
¢ŚČĖĢåŃĄöø³öŃŖ”¢»¼»µŃŖ²”µÄŌŅņÖ÷ŅŖŹĒŅņĪŖȱ·¦______(Ģī”°Ī¬ÉśĖŲA”±”¢”°Ī¬ÉśĖŲC”±»ņ”°Ī¬ÉśĖŲD”±)”£
(3)ŠŌÄÜø÷ŅģµÄø÷ÖÖ²ÄĮĻµÄ¹ć·ŗÓ¦ÓĆ“ó“óĢįøßĮĖČĖĆĒµÄÉś»īĖ®Ę½”£ŹŌ»Ų“šĪŹĢā£ŗ

¢ŁŹÆÄ«Ļ©(¼ūĶ¼)æÉÓĆ×÷Ģ«ŃōÄܵē³ŲµÄµē¼«£¬ÕāĄļÖ÷ŅŖĄūÓĆĮĖŹÆÄ«Ļ©µÄ______ŠŌ”£
¢ŚøßĀÆĮ¶ĢśŗĶÉś²ś¹čĖįŃĪĖ®Äą¶¼ŅŖÓƵ½µÄŌĮĻŹĒ______(Ģī×ÖÄø)”£
a. š¤ĶĮ””””””””””””b. ŹÆ»ŅŹÆ””””””””””””c. ½¹Ģæ
¢Ū”°ÉńĘß”±¹ś²ś”°·ÉĢģ”±²ÕĶā·žÓÉĮł²ć×é³É”£“ÓÄŚµ½ĶāŅĄ“ĪĪŖÓÉĢŲŹā·Ą¾²µē“¦Ąķ¹żµÄĆŽ²¼×é³ÉµÄŹęŹŹ²ć”¢ŗĻ³ÉĻš½ŗÖŹµŲµÄ±ø·ŻĘųĆÜ²ć”¢ø“ŗĻ²ÄĮĻ½į¹¹×é³ÉµÄÖ÷ĘųĆÜ²ć”¢µÓĀŚĆęĮĻµÄĻŽÖĘ²ć”¢øōČČ²ćŗĶ×īĶā·Ą»¤²ć”£ĘäÖŠÓÉĢģȻӊ»śøß·Ö×Ó²ÄĮĻ×é³ÉµÄ²ćŹĒ______(Ģī×ÖÄø)”£
a. ŹęŹŹ²ć b. ±ø·ŻĘųĆܲć c. Ö÷ĘųĆܲć
¢Ü²ÄĮĻÓė»ÆѧĆÜĒŠĻą¹Ų£¬±ķÖŠ¶ŌÓ¦¹ŲĻµÕżČ·µÄŹĒ______(Ģī×ÖÄø)”£
Ń”Ļī | ²ÄĮĻ | Ö÷ŅŖ»Æѧ³É·Ö |
a | øÕÓń”¢½šøÕŹÆ | ČżŃõ»Æ¶žĀĮ |
b | “óĄķŹÆ”¢ŹÆ»ŅŹÆ | Ģ¼ĖįøĘ |
c | ¹āµ¼ĻĖĪ¬”¢ĘÕĶز£Į§ | ¹čĖįŃĪ |
¢ŻĶĘ÷±ķĆęÓŠŹ±»įÉś³ÉĶĀĢ[Cu2(OH)2CO3]£¬Õā²ćĶĀĢæÉÓĆŃĪĖį³żČ„£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½________________________________”£
B”¶ÓŠ»ś»Æѧ»ł“””·
(1)ČĻŹ¶ÓŠ»ś»ÆŗĻĪļµÄ½į¹¹ÓėĄą±šÓŠÖśÓŚĄķ½āĘäŠŌÖŹ”£
¢ŁĻĀĮŠÓŠ»ś»ÆŗĻĪļÓė±½¼×Ėį(C6H5COOH)»„ĪŖĶ¬ĻµĪļµÄŹĒ______(Ģī×ÖÄø£¬ĻĀĶ¬)”£
a. C6H5CH2COOH b. C6H5CH2CHO c. C6H5OH
¢ŚĻĀĮŠÓŠ»ś»ÆŗĻĪļŅ×ČÜÓŚĖ®µÄŹĒ______”£
a. ±½”””” b. ŅŅĶé”””” c. ŅŅ“¼
¢ŪĻĀĮŠŹŌ¼ĮæÉÓĆÓŚ¼ų±šŅŅĖįŗĶŅŅČ©µÄŹĒ______”£
a. Ė® b. Ņų°±ČÜŅŗ c. Ļ”ĮņĖį
(2)±āĢŅĖį(C6H5CHOHCOOH)ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ”£
¢Ł±āĢŅĖį·Ö×ÓÖŠÓŠ______ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒā”£
¢Ś±āĢŅĖįÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘĪŖ______ŗĶ______”£
¢Ū1 mol±āĢŅĖį×ī¶ąÄÜÓė______mol½šŹōÄĘ·“Ó¦
(3)»ÆŗĻĪļCŹĒŅ»ÖÖŅ½Ņ©ÖŠ¼äĢ壬æÉĶعżĻĀĮŠ·½·ØŗĻ³É£ŗ
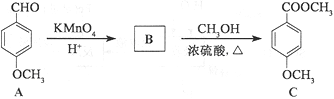
¢ŁAÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘĪŖ______ŗĶ______”£
¢ŚBµÄ½į¹¹¼ņŹ½ĪŖ______”£
¢ŪB”śCµÄ·“Ó¦ĄąŠĶĪŖ______”£
¢ÜCµÄĶ¬·ÖŅģ¹¹ĢåDÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ÄÜÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£¬ĒŅ1molD×ī¶ąÄÜÓė2molNaOH·“Ó¦”£D·Ö×ÓÖŠÓŠ4ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒā£¬ĒėŠ“³öDµÄŅ»ÖÖ½į¹¹¼ņŹ½£ŗ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½³ĢŹ½ÖŠ£¬ÕżČ·µÄŹĒ£Ø £©
A.ŹÆ»ŅŹÆÓėŃĪĖį·“Ó¦£ŗCaCO3£«2H£«£½Ca2£«£«CO2”ü£«H2O
B.ÄĘÓėĖ®µÄ·“Ó¦£ŗ![]()
C.ĒāŃõ»ÆĶČÜÓŚŃĪĖį£ŗCu2£«£«2OH££«2H£«£½Cu2£«£«2H2O
D.ĀČĘųÓėĖ®µÄ·“Ó¦£ŗ Cl2£«H2O £½ 2H£«£«Cl££«ClO”Ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¾ŻĻĀĮŠŠÅĻ¢Ķź³ÉĖłŠč»Ų“šµÄĪŹĢā£ŗ
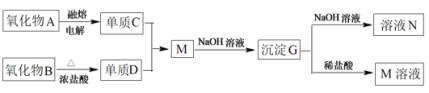
ĘäÖŠŃõ»ÆĪļAŹĒ°×É«¹ĢĢ壻Ńõ»ÆĪļBŹĒŗŚÉ«¹ĢĢ壻µ„ÖŹDĪŖÓŠ¶¾µÄ»ĘĀĢÉ«ĘųĢ壬µ„ÖŹC²»ČÜÓŚĄäµÄÅØĻõĖį”£
£Ø1£©DŹĒ_______£»GŹĒ_______£ØĢī»ÆѧŹ½£©
£Ø2£©Š“³öĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗM+NaOHČÜŅŗÉś³ÉG_____________________”¢G+NaOHČÜŅŗÉś³ÉN______________________________________________________”£
£Ø3£©µ„ÖŹC²»ČÜÓŚĄäµÄÅØĻõĖįµÄŌŅņŹĒ____________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆČēĶ¼ĖłŹ¾×°ÖĆæÉŅŌ½ųŠŠµē¶Ę£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ

A. µē¶ĘŹ±“ż¶ĘµÄ½šŹōÖĘĘ·×÷Ņõ¼«£¬¶Ę²ć½šŹō×÷Ńō¼«
B. ÓĆŗ¬ÓŠ¶Ę²ć½šŹōĄė×ÓµÄČÜŅŗ×öµē¶ĘŅŗ
C. ½«“ż¶ĘĢś¼žøÄĪŖ“ÖĶ°å£¬¼“æɽųŠŠĶµÄ¾«Į¶
D. µē¶Ę·ĻĖ®ÅÅ·ÅĒ°±ŲŠė¾¹ż“¦Ąķ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ²ā¶Ø![]() ČÜŅŗĻČÉżĪĀŌŁ½µĪĀ¹ż³ĢÖŠµÄ
ČÜŅŗĻČÉżĪĀŌŁ½µĪĀ¹ż³ĢÖŠµÄ![]() £¬Źż¾ŻČēĻĀ±ķ”£ŹµŃé¹ż³ĢÖŠ£¬Č”¢Ł”¢¢ÜŹ±æĢµÄČÜŅŗ£¬¼ÓČėŃĪĖįĖį»ÆµÄ
£¬Źż¾ŻČēĻĀ±ķ”£ŹµŃé¹ż³ĢÖŠ£¬Č”¢Ł”¢¢ÜŹ±æĢµÄČÜŅŗ£¬¼ÓČėŃĪĖįĖį»ÆµÄ![]() ČÜŅŗ×ö¶Ō±ČŹµŃ飬¢Ü²śÉś°×É«³Įµķ¶ą”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
ČÜŅŗ×ö¶Ō±ČŹµŃ飬¢Ü²śÉś°×É«³Įµķ¶ą”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
Ź±æĢ | ¢Ł | ¢Ś | ¢Ū | ¢Ü |
ĪĀ¶Č | 25 | 30 | 40 | 25 |
| 9.66 | 9.52 | 9.37 | 9.25 |
A. ![]() ČÜŅŗÖŠ“ęŌŚĖ®½āĘ½ŗā£ŗ
ČÜŅŗÖŠ“ęŌŚĖ®½āĘ½ŗā£ŗ![]()
B. ¢Ü²śÉśµÄ°×É«³ĮµķŹĒ![]()
C. ¢Ł”ś¢ŪµÄ¹ż³ĢÖŠ£¬![]() ŌŚ½µµĶ
ŌŚ½µµĶ
D. ¢Ł”ś¢ŪµÄ¹ż³ĢÖŠ,ĪĀ¶ČÓė![]() Ļą±Č£¬Ē°Õ߶ŌĖ®½āĘ½ŗāµÄÓ°Ļģøü“ó
Ļą±Č£¬Ē°Õ߶ŌĖ®½āĘ½ŗāµÄÓ°Ļģøü“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææÉÄę·“Ó¦![]()
![]() ŌŚĘ½ŗāŅĘ¶ÆŹ±µÄŃÕÉ«±ä»ÆæÉŅŌÓĆĄ“ÖøŹ¾·ÅČČ¹ż³ĢŗĶĪüČČ¹ż³Ģ”£ĻĀĆęŹĒijĶ¬Ń§µÄ²æ·ÖŹµŃé±Øøę”£
ŌŚĘ½ŗāŅĘ¶ÆŹ±µÄŃÕÉ«±ä»ÆæÉŅŌÓĆĄ“ÖøŹ¾·ÅČČ¹ż³ĢŗĶĪüČČ¹ż³Ģ”£ĻĀĆęŹĒijĶ¬Ń§µÄ²æ·ÖŹµŃé±Øøę”£
| 1.Ļņ¼×ÉÕ±ÖŠ¼ÓČė 2.ĻņŅŅÉÕ±ÖŠĶ¶ČėŅ»¶ØĮæµÄ |
£Ø1£©¼×ÉÕ±ÖŠ![]() ĒņµÄŗģ×ŲÉ«±äĒ³£¬ĖµĆ÷Ę½ŗā
ĒņµÄŗģ×ŲÉ«±äĒ³£¬ĖµĆ÷Ę½ŗā![]() Ļņ______________£ØĢī”°Õż·“Ó¦”±»ņ”°Äę·“Ó¦”±£©·½ĻņŅĘ¶Æ£¬ĖłŅŌ
Ļņ______________£ØĢī”°Õż·“Ó¦”±»ņ”°Äę·“Ó¦”±£©·½ĻņŅĘ¶Æ£¬ĖłŅŌ![]() ¾§ĢåČÜÓŚĖ®ŹĒ__________________£ØĢī”°·ÅČČ”±»ņ”°ĪüČČ”±£©¹ż³Ģ”£
¾§ĢåČÜÓŚĖ®ŹĒ__________________£ØĢī”°·ÅČČ”±»ņ”°ĪüČČ”±£©¹ż³Ģ”£
£Ø2£©øł¾ŻŅŅÉÕ±ÖŠµÄĻÖĻ󣬲¹Č«![]() Óė
Óė![]() ·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»ÆŹ¾ŅāĶ¼_____”£
·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»ÆŹ¾ŅāĶ¼_____”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ŹĒÉĮŠææó£ØÖ÷ŅŖ³É·ÖŹĒ![]() £¬ŗ¬ÓŠÉŁĮæ
£¬ŗ¬ÓŠÉŁĮæ![]() £©Öʱø
£©Öʱø![]() µÄŅ»ÖÖ¹¤ŅÕĮ÷³Ģ£ŗ
µÄŅ»ÖÖ¹¤ŅÕĮ÷³Ģ£ŗ
![]()
׏ĮĻ£ŗĻą¹Ų½šŹōĄė×ÓÅضČĪŖ![]() Ź±ŠĪ³ÉĒāŃõ»ÆĪļ³ĮµķµÄ
Ź±ŠĪ³ÉĒāŃõ»ÆĪļ³ĮµķµÄ![]() ·¶Ī§ČēĻĀ£ŗ
·¶Ī§ČēĻĀ£ŗ
½šŹōĄė×Ó |
|
|
|
æŖŹ¼³ĮµķµÄ | 1.5 | 6.3 | 6.2 |
³ĮµķĶźČ«µÄ | 2.8 | 8.3 | 8.2 |
£Ø1£©ÉĮŠææóŌŚČܽžÖ®Ē°»į½«Ęä·ŪĖ飬ÄæµÄŹĒ______________”£
£Ø2£©Čܽž¹ż³ĢŹ¹ÓĆ¹żĮæµÄ![]() ČÜŅŗŗĶ
ČÜŅŗŗĶ![]() ½žČ”æó·Ū£¬·¢ÉśµÄÖ÷ŅŖ·“Ó¦ŹĒ£ŗ
½žČ”æó·Ū£¬·¢ÉśµÄÖ÷ŅŖ·“Ó¦ŹĒ£ŗ
![]() ”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ____________£ØĢī×ÖÄøŠņŗÅ£©”£
”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ____________£ØĢī×ÖÄøŠņŗÅ£©”£
a.½ž³öŅŗÖŠŗ¬ÓŠ![]() µČŃōĄė×Ó
µČŃōĄė×Ó
b.¼ÓČėĮņĖį£¬æÉŅŌŅÖÖĘ![]() Ė®½ā
Ė®½ā
c.ČōøÄÓĆ![]() ČÜŅŗ½ųŠŠ½žČ”£¬½«·¢Éś·“Ó¦£ŗ
ČÜŅŗ½ųŠŠ½žČ”£¬½«·¢Éś·“Ó¦£ŗ![]()
£Ø3£©¹¤Ņµ³żĢś¹ż³ĢŠčŅŖæŲÖĘ³ĮµķĖŁĀŹ£¬Ņņ“Ė·ÖĪŖ»¹ŌŗĶŃõ»ÆĮ½²½ĻČŗó½ųŠŠ£¬ČēĻĀĶ¼”£»¹Ō¹ż³Ģ½«²æ·Ö![]() ×Ŗ»ÆĪŖ
×Ŗ»ÆĪŖ![]() £¬µĆµ½
£¬µĆµ½![]() Š”ÓŚ1.5µÄČÜŅŗ”£Ńõ»Æ¹ż³ĢĻņČÜŅŗÖŠĻČ¼ÓČėŃõ»ÆĪļa£¬ŌŁĶØČė
Š”ÓŚ1.5µÄČÜŅŗ”£Ńõ»Æ¹ż³ĢĻņČÜŅŗÖŠĻČ¼ÓČėŃõ»ÆĪļa£¬ŌŁĶØČė![]() ”£
ӣ
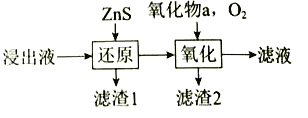
¢ŁaæÉŅŌŹĒ______________£¬¼ÓČėaµÄ×÷ÓĆŹĒ_______________”£
¢Ś³żĢś¹ż³ĢÖŠæÉŅŌæŲÖĘČÜŅŗÖŠ![]() µÄ²Ł×÷ŹĒ_______________”£
µÄ²Ł×÷ŹĒ_______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æX”¢Y”¢Z”¢R”¢WŹĒŌ×ÓŠņŹżŅĄ“ĪµŻŌöµÄĪåÖÖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬ĖüĆĒĖłŌŚÖÜĘŚŹżÖ®ŗĶĪŖ11£¬ĘäÖŠYŌŖĖŲ×īøßÓė×īµĶ»ÆŗĻ¼ŪµÄ“śŹżŗĶĪŖ2£¬YŗĶZµÄµ„ÖŹÉś³ÉµÄ»ÆŗĻĪļŹĒŅ»ÖÖ“«µŻÉń¾ŠÅĻ¢µÄ”°ŠÅŹ¹·Ö×Ó”±£¬RµÄŌ×Ó°ė¾¶ŹĒĪåÖÖŌŖĖŲÖŠ×ī“óµÄ£¬YŗĶWŹĒĶ¬×åŌŖĖŲ”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø £©
A. ¼ņµ„Ąė×ӵĻ¹ŌŠŌ£ŗY>Z
B. RµÄµ„ÖŹæÉÄÜŹĒ½šŹō»ņ·Ē½šŹō
C. ÓÉX”¢ZŗĶW¹¹³ÉµÄĖįŅ»¶ØŹĒČżŌŖĖį
D. ±ź×¼×“æöĻĀ£¬1molYZÓė0.5mol![]() »ģŗĻŗóĖłµĆĘųĢåµÄĢå»żŅ»¶ØŠ”ÓŚ22.4L
»ģŗĻŗóĖłµĆĘųĢåµÄĢå»żŅ»¶ØŠ”ÓŚ22.4L
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com