
【题目】易燃、易爆等危险化学品的包装应标有相应警告标志。浓硫酸包装上的标志为
A. 腐蚀品B. 易燃品C. 剧毒品D. 爆炸品
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.物质的量浓度相同的溶液中所含溶质的微粒数相同
B.常温常压下,0.1molH2气体约含6.02×1022个H2分子
C.1molL﹣1醋酸溶液100mL中H+的个数约为0.1NA
D.标准状况下,1molH2O的体积约22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】市场上出售的饮料各种各样,有不法商贩为增加饮料口感和粘稠度,在饮料中加塑化剂,塑化剂的分子式为C16H22O4 ,不能作为食品添加剂。塑化剂属于
A. 单质 B. 氧化物 C. 无机物 D. 有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【选修3:物质的结构与性质】Ⅰ.氟元素是电负性最大的非金属元素,且氟原子的半径小,因此氟单质极易和金属单质反应且把它们氧化到最高价态,如MnF7 、VF5 、CaF2 等。氟元素还可以和氧元素形成氟化物,如OF2 等。
请回答下列问题:

(1)V原子的核外电子排布式为 。如图表示一个不完整的CaF2 晶胞,则图中实心球表示 (填“F-或Ca2+ )。 设晶胞边长为a,则最近的F-和Ca2+之间的距离为 (用含a的代数式表示)。
(2)OF2 分子中氧原子的轨道杂化类型为 ,OF2被称为氟化物而不被称为氧化物的原因是 。
Ⅱ.纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2的化合物。回答下列问题:
(3)写出基态Cu+ 的核外电子排布式 。C、N、O三种元素的第一电离能由大到小的顺序是 。
(4)如图所示是铜的某种氧化物的晶胞示意图,该氧化物的化学式为 。
(5)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,在滴加氨水至沉淀刚全部溶解时可得到蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[Cu(NH3)4]SO4·H2O沉淀。该深蓝色沉淀中的NH3通过键与中心离子Cu2+结合。NH3分子中的N原子杂化方式是 。与NH3分子互为等电子体的一种微粒是 (任写一种)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(g)+xB(g)![]() 2C(g),2 min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果正确的是
2C(g),2 min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果正确的是
A. 平衡时,物质的量之比n(A)∶n(B)∶n(C)=2∶11∶4
B. x值等于3
C. A的转化率为20%
D. B的平均反应速率为0.4 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组用HNO3 与大理石反应过程中质量减小的方法研究影响反应速率的因素。所用HNO3浓度为1.00mol/L、2.00mol/L,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HN03 的用量为25.0mL、大理石用量为10.00g。
(1)请完成以下实验设计表,在实验目的一栏中填出对应的实验编号:
试验编号 | T/K | 大理石规格 | HNO3浓度mol/L | 实验目的 |
① | 298 | 粗颗粒 | 2.00 | 实验①和②探究HNO3 浓度对该反应速率的影响; (II)实验①和____探究温度对该反应速率的影响; (III)实验①和____探究大理石规格(粗、细)对该反应速率的影响。 |
② | 298 | 粗颗粒 | 1.00 | |
③ | 308 | 粗颗粒 | 2.00 | |
④ | 298 | 细颗粒 | 2.00 |
(2)实验①中CO2质量随时间变化的关系见图:
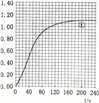
依据反应方程式CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O,计算实验①在70~90s范围内HNO3的平均反应速率_______。(忽略溶液体积变化)
(3)请在上图中,画出实验②和③中CO2质量随时间变化关系的预期结果示意图,并标出线的序号_______。
(4)工业上己实现CO2和H2反应生成甲醇的转化。己知:在一恒温、恒容密闭容器中充入1mol CO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。测得CO2和CH3OH (g)的浓度随时间变化如下图所示。请回答:

①达到平衡时H2的转化率为_______。在前10min内,用CO2表示的反应速率:V(CO2)=______mol/(L·min)
②能判断该反应达到化学平衡状态的依据是_______。
a.容器压强不变 b.混合气体中c(CO2)不变
c. v(CH3OH)=v(H2O) d. c(CH3OH)=c(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分离方法不正确的是( )
A.用结晶的方法分离汽油和水
B.用过滤的方法除去氯化钠溶液中的泥沙
C.用重结晶的方法从含有少量氯化钠的硝酸钾溶液中提取硝酸钾
D.蒸馏法分离乙酸(沸点118)和乙酸乙酯(沸点77.1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴及其化合物可应用与催化剂、电池、颜料与染料等。
(1)CoO是一种油漆添加剂,可通过反应①②制备。
①2Co(s)+O2(g)=2CoO(s) ΔH1=akJ·mol-1
②2CoCO3(s) =CoO(s) + CO2 (g) ΔH2=akJ·mol-1
则反应2Co(s)+O2(g)+2CO2(g)=2CoO3(s) 的ΔH=_________。
(2)某锂电池的电解质可传导Li+,电池反应式为:LiC6+CoO2![]() C6+LiCoO2
C6+LiCoO2
①电池放电时,负极的电极反应式为_________,Li+向______移动(填“正极”或“负极“)。
②一种回收电极中Co元素的方法是:将LiCoO2与H2O2、H2SO4反应生成CoSO4。该反应的化学方程式为___________________。
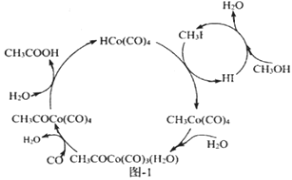
(3)BASF高压法制备醋酸采用钴碘催化循环过程如图-1所示,该循环的总反应方程式为_________________(反应条件无需列出)
(4)某含钴催化剂可同时催化去除柴油车尾气中的碳烟(C)和NOx。不同温度下,将10mol模拟尾气(成分如下表所示)以相同的流速通过该催化剂,测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图-2所示.
模拟尾气 | 气体 | 碳烟 | ||
NO | O2 | He | ||
物质的量分数或物质的量 | 0.25% | 5% | 94.75% | a mol |
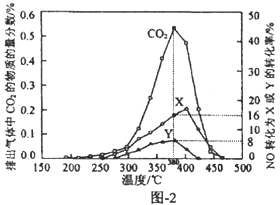
①380℃时,测得排出的气体中含0.45 mol O2和0.0525 mol CO2,则Y的化学式为__________________。
②实验过程中采用NO模拟NOx,,而不采用NO2的原因是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com