
| A、金属Al无剩余 |
| B、c(Na+)=c(AlO-2) |
| C、生成气体为2mol |
| D、c(Na+)=c(Al3+) |
| 4 |
| 2 |


科目:高中化学 来源: 题型:
A、硝基苯的结构简式是: |
B、乙炔的电子式是: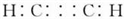 |
C、乙醚分子的球棍模型是: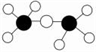 |
| D、甲酸中存在-CHO和-COOH两种官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲烷与氯气混合,光照一段时间后黄绿色消失 |
| B、乙烯使酸性高锰酸钾溶液褪色 |
| C、将苯滴入少量到溴水中,振荡后水层接近无色 |
| D、乙烯使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、(1-a%)×
| ||
B、a%×
| ||
| C、1-a% | ||
| D、(1-13a%/12) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入硫酸钾溶液 |
| B、加入几滴硫酸铜溶液 |
| C、改用热的2mol/L硫酸溶液 |
| D、改用浓硫酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com