
| A、升高温度,平衡将正向移动 | ||
B、X的正反应速率是Y的逆反应速率的
| ||
| C、降低温度,混合气体的平均相对分子质量变小 | ||
| D、增加X的物质的量,Y的转化率降低 |
| m |
| n |
| m |
| n |
| m |
| n |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+
| ||||
| B、Ca(HCO3)2溶液与过量NaOH溶液反应 HCO3-+OH-+Ca2+═CaCO3↓+H2O | ||||
| C、氢氧化铁溶于氢碘酸溶液:Fe(OH)3+3H+═Fe3++3H2O | ||||
| D、等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3?H2O+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、+1 | B、+2 | C、+3 | D、+4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②⑥ | B、②⑤ |
| C、①②⑤⑥ | D、②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 待提纯物 | 杂质 | 试剂及主要操作方法 |
| A | 苯 | 溴单质 | 加苯酚,过滤 |
| B | 甲苯 | 苯甲酸 | 饱和NaHCO3溶液,分液 |
| C | 甲烷 | 乙烯 | 通入酸性高锰酸钾溶液,洗涤 |
| D | 乙醛 | 乙酸 | 加入氢氧化钠溶液,分液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、恒温恒容,充入N2O5气体,其转化率增大 |
| B、加压,平衡向逆反应方向移动,混合气体颜色变浅 |
| C、若平衡常数增大,则一定是升高了温度 |
| D、当v正(N2O5)=2v逆(NO2)时,反应达到化学平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
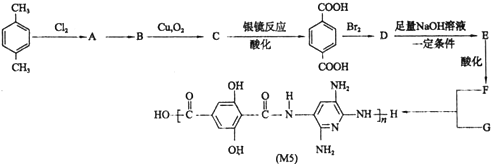
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com