

| 1 |
| 8 |
| 1 |
| 2 |


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
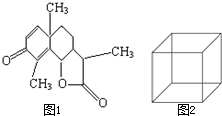 (1)图1是一种驱蛔虫药--山道年的结构简式,试确定其分子式为:
(1)图1是一种驱蛔虫药--山道年的结构简式,试确定其分子式为:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 有A、B、C、D、E五种元素(A、B、C、D、E分别代表元素符号),其中A元素原子核内只有一个质子;B元素的基态原子s亚层的总电子数比p亚层的总电子数多1;C元素的原子最外层电子数是次外层电子数的3倍;D位于B的下一周期,在同周期元素形成的简单离子中,D形成的简单离子半径最小;E的基态原子中电子排布在三个能级上,且这三个能级所含电子数均相同.
有A、B、C、D、E五种元素(A、B、C、D、E分别代表元素符号),其中A元素原子核内只有一个质子;B元素的基态原子s亚层的总电子数比p亚层的总电子数多1;C元素的原子最外层电子数是次外层电子数的3倍;D位于B的下一周期,在同周期元素形成的简单离子中,D形成的简单离子半径最小;E的基态原子中电子排布在三个能级上,且这三个能级所含电子数均相同.查看答案和解析>>
科目:高中化学 来源: 题型:
| 共价键 | Cl-Cl | Br-Br | I-I | H-Cl | H-Br | H-I | H-H |
| 键能(kJ/mol) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学药品着火,都要立即用水或泡沫灭火器灭火 |
| B、开发和推广新能源是实现低碳生活的途径之一 |
| C、食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质 |
| D、纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
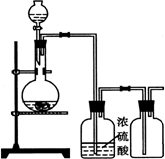
| A、氯化钠固体与浓硫酸制氯化氢 |
| B、铜和稀硝酸制一氧化氮 |
| C、锌和稀硫酸制氢气 |
| D、用生石灰和浓氨水制氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+ |
| B、Cl- |
| C、CO32- |
| D、OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com