
【题目】过氧化钙(CaO2)是一种白色晶体,极微溶于水,不溶于醇类。可与水缓慢反应,易与酸反应。实验室通常用CaCl2在碱性条件下与H2O2反应制得(该反应剧烈并大量放热),装置如图所示,请回答下面的问题:
I.CaO2的制备

(1)漏斗在使用时其上口的玻璃塞应________(填“打开”或“关闭”),支管B的作用是________。
(2)将盛有浓CaCl2溶液的装置置于冰水混合物中。其原因是:使反应平稳进行、___________。
(3)加入H2O2与浓氨水的混合溶液,使反应开始。
①反应的化学方程式是_______________。
②滴加H2O2与浓氨水混合溶液之前,还应进行的操作是______。
(4)待反应结束后,经______(填操作)得CaO2粗产品。
Ⅱ.CaO2纯度的测定:将一定量的CaO2溶于稀硫酸,用标准KMnO4溶液滴定生成的H2O2(KMnO4反应后生成Mn2+),计算确定CaO2的含量。
(5)现每次称取0.4000g样品溶解后,用0.1000mol/L的KMnO4溶液滴定,所得的数据如下表所示,则样品的纯度__________。
实验序号 | ① | ② | ③ | ④ |
消耗KMnO4体积/mL | 19.98 | 20.02 | 20.20 | 20.00 |
(6)测得CaO2样品的纯度偏低,其原因可能是______(选填编号)。
A.烘烤时间不足
B.配制KMnO4标准溶液定容时俯视容量瓶刻度线
C.在洁净干燥的酸式滴定管中未润洗即装标准液
D.滴定前尖嘴部分有气泡,滴定后消失
【答案】 关闭 平衡压强,使恒压滴液漏斗中的液体能够顺利滴下 防止双氧水分解、氨气逸出、温度降低过氧化钙的溶解度变低(合理答案均得分) CaCl2+ H2O2+ 2NH3·H2O= CaO2↓+ 2H2O+ 2NH4C1 冷凝管接通自来水 过滤 90.00% AB
【解析】(1)该实验中使用的是恒压滴液漏斗,在使用时其上口的玻璃塞应关闭,支管B可以平衡压强,使恒压滴液漏斗中的液体能够顺利滴下,故答案为:关闭;平衡压强,使恒压滴液漏斗中的液体能够顺利滴下;
(2)CaCl2在碱性条件下与H2O2反应制得(该反应剧烈并大量放热),将盛有浓CaCl2溶液的装置置于冰水混合物中,可以使反应平稳进行、同时防止双氧水分解、氨气逸出、温度降低过氧化钙的溶解度变低,故答案为:防止双氧水分解、氨气逸出、温度降低过氧化钙的溶解度变低;
(3)①加入H2O2与浓氨水的混合溶液,反应生成CaO2沉淀,反应的化学方程式为CaCl2+ H2O2+ 2NH3·H2O= CaO2↓+ 2H2O+ 2NH4C1,故答案为:CaCl2+ H2O2+ 2NH3·H2O= CaO2↓+ 2H2O+ 2NH4C1;
②CaCl2在碱性条件下与H2O2反应制得(该反应剧烈并大量放热),滴加H2O2与浓氨水混合溶液之前,需要将冷凝管接通自来水,故答案为:冷凝管接通自来水;
(4)过氧化钙(CaO2)是一种白色晶体,极微溶于水,不溶于醇类,待反应结束后,经过滤即可得CaO2粗产品,故答案为:过滤;
(5)根据表中消耗高锰酸钾溶液的体积数据可知,第三次数据与其它三组误差较大,应该舍弃;则滴定中消耗酸性高锰酸钾的平均体积为:![]() mL=20.00mL,每次滴定消耗的高锰酸钾的物质的量为:n(KMnO4)=0.1000mol/L×0.02L=0.002mol,
mL=20.00mL,每次滴定消耗的高锰酸钾的物质的量为:n(KMnO4)=0.1000mol/L×0.02L=0.002mol,
KMnO4反应后生成Mn2+,化合价降低7-2)=5价,CaO2被氧化成氧气,化合价从-1升高到0价,至少升高:[0-(-1)]×2=2,根据化合价升降相等可得反应的关系式:2KMnO4~5CaO2,则每次称取0.4000g样品中含有的过氧化钙的物质的量为:n(CaO2)=![]() ×n(KMnO4)=0.002mol×
×n(KMnO4)=0.002mol×![]() =0.005mol,所以该样品中过氧化钙的纯度为:
=0.005mol,所以该样品中过氧化钙的纯度为:![]() ×100%=90.00%,故答案为:90.00%;
×100%=90.00%,故答案为:90.00%;
(6)A.烘烤时间不足,样品中含有杂质水分,导致样品中过氧化钙的纯度偏小,故A正确;B.配制KMnO4标准溶液定容时俯视容量瓶标线,导致标准液浓度偏高,滴定过程中营养样品中过氧化钙的物质的量不变,则消耗的标准液体积偏小,测定的过氧化钙的纯度偏小,故B正确;C.在洁净干燥的酸式滴定管中未润洗即装标准液,标准液被蒸馏水稀释,滴定时消耗的标准液体积偏大,计算出的过氧化钙的纯度偏大,故C错误;D.滴定前尖嘴处有气泡,滴定后消失,导致消耗的标准液体积偏大,根据关系式计算出的过氧化钙的质量偏大,过氧化钙的纯度偏高,故D错误;故答案为:AB。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列叙述中正确的是( )
A. 已知N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4 kJ·mol-1,当在一定温度压强下向一密闭容器中充入0.5molN2、1.5molH2使其充分反应,其反应放出的热量为46.2 kJ
2NH3(g) △H=-92.4 kJ·mol-1,当在一定温度压强下向一密闭容器中充入0.5molN2、1.5molH2使其充分反应,其反应放出的热量为46.2 kJ
B. 常温常压下,7.1gCl2与足量铁充分反应,转移的电子数为0.2NA
C. 室温下,1LpH=13的NaOH溶液中,由水电离的OH-数目为0.1NA
D. 12g金刚石晶体中含有的碳碳键数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器中进行反应:mX(g)+nY(g) ![]() pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示: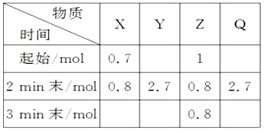
已知2 min内v(Q)=0.075 mol·L-1·min-1 , v(Z)∶v(Y)=1∶2。
(1)试确定:起始时n(Y)= , n(Q)=。
(2)方程式中m= , n= , p= , q=。
(3)用Z表示2 min内的反应速率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2(g)+O2(g) ![]() 2SO3(g) △H<0一定条件下在某密闭容器中达到平衡。t1时改变某一条件,反应速率与时间关系如下图。下列说法中正确的是( )
2SO3(g) △H<0一定条件下在某密闭容器中达到平衡。t1时改变某一条件,反应速率与时间关系如下图。下列说法中正确的是( )
A.维持温度、反应体系体积不变,t1时充入SO3(g)
B.维持压强不变,t1时升高反应体系温度
C.维持温度不变,t1时扩大反应体系体积
D.维持温度、容器体积不变,t1时充入SO3(g),同时减少SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关胶体的说法不正确的是( )
A.氢氧化铁胶体具有吸附性,可做净水剂
B.向FeCl3溶液中滴加NaOH溶液,可制得Fe(OH)3胶体
C.可用丁达尔效应鉴别氢氧化铁胶体和水
D.盐卤点豆腐、江河入海口处“三角洲”的形成、高压直流电除烟尘均与胶体的性质有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A.已知2SO2(g)+O2![]() 2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量
2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量
B.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定
C.已知H+(aq)+OH-(aq)=H2O(1),△H=-57.3kJ/mol,则任何酸碱中和反应的热效应均为57.3 kJ
D.已知2C(s)+2O2(g)=2CO2(g) △H1 , 2C(s)+O2(g)=2CO(g) △H2 则△H1<△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1 mol/L CH3COOH溶液中存在如下电离平衡:CH3COOH ![]() CH3COO-+H+ , 对于该平衡,下列叙述正确的是( )
CH3COO-+H+ , 对于该平衡,下列叙述正确的是( )
A.加入水时,平衡逆向移动
B.加入少量NaOH固体,平衡正向移动
C.加入少量0.1 mol/L HCl溶液,溶液中c(H+)不变
D.加入少量CH3COONa固体,平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中只含有Al3+、Na+、Cl-、SO42-四种离子,已知前三种离子的个数比为3:3:2,则溶液中Na+和SO42-的离子个数比为 ( )
A.2:1B.2:5C.3:5D.3:4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com