
| A.原子半径:甲<乙<丙 |
| B.最外层电子数:丙>丁 |
| C.若甲、乙、丙均是金属,则氢氧化物碱性:甲<乙<丙 |
| D.若乙的最高价含氧酸为强酸,则丙是活泼非金属元素 |
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案科目:高中化学 来源:不详 题型:单选题
| A.RO | B.R2O3 | C.RO2 | D.R2O5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熔沸点:F2<Cl2<Br2<I2 | B.颜色:F2、Cl2、Br2、I2逐渐加深 |
| C.还原性:F– > Cl–> Br– > I– | D.热稳定性:HF>HCl>HBr>HI |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 、D、E、F、G、H是元素周期表中八种原子序数依次增大的短周期元素。
、D、E、F、G、H是元素周期表中八种原子序数依次增大的短周期元素。 电离的是 (各写一种化学式);
电离的是 (各写一种化学式);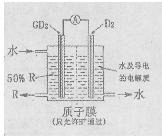
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.使阴、阳离子结合成化合物的静电作用叫做离子键 |
| B.金属元素与非金属元素相化合时一定形成离子键 |
| C.在化学反应中,某元素由化合态变为游离态,该元素被还原 |
D.失电子难的原子获得电子的能力一 定强 定强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③④ | B.①③ | C.①②③④ | D.②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com