
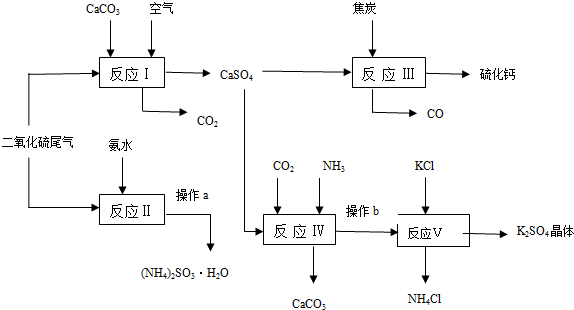
分析 由流程可知,I中发生2CaCO3+O2+2SO2=2CaSO4+2CO2,反应Ⅳ为NH4HCO3、CaSO4、NH3反应生成碳酸钙和硫酸铵,发生NH4HCO3+NH3+CaSO4=CaCO3↓+(NH4)2SO4,可知CaCO3、CO2可循环使用,反应Ⅴ为硫酸铵溶液中加入氯化钾生成硫酸钾晶体,所以操作b为过滤,滤液中含有的阳离子为铵根离子,Ⅱ中发生SO2+2NH3.H2O=(NH4)2SO3+H2O,Ⅲ中发生CaSO4+4C=CaS+4CO↑,
(1)煤300t(煤中含硫的质量分数为2.5%)中含有硫元素的质量为7.5t,根据硫元素守恒有关系式根据关系式S~SO2~CaSO4•2H2O,可计算出生产石膏的质量;
(2)操作a是从亚硫酸铵溶液中获得亚硫酸铵晶体,亚硫酸铵晶体受热易分解,据此分析;
(3)反应Ⅲ化学方程式为:CaSO4+4C=CaS+4CO↑,氧化剂为CaSO4,还原剂为C;
(4)反应Ⅳ为NH4HCO3、CaSO4、NH3反应生成碳酸钙和硫酸铵,操作b所得滤液中阳离子为铵根离子,用碱和石蕊试纸检验铵根离子;
(5)硫酸钾在不同溶剂中溶解度的不同,以此分析达到析出晶体的目的;
(6)根据上面的分析可知,循环使用的物质.
解答 解:由流程可知,I中发生2CaCO3+O2+2SO2=2CaSO4+2CO2,反应Ⅳ为NH4HCO3、CaSO4、NH3反应生成碳酸钙和硫酸铵,发生NH4HCO3+NH3+CaSO4=CaCO3↓+(NH4)2SO4,可知CaCO3、CO2可循环使用,反应Ⅴ为硫酸铵溶液中加入氯化钾生成硫酸钾晶体,所以操作b为过滤,滤液中含有的阳离子为铵根离子,Ⅱ中发生SO2+2NH3.H2O=(NH4)2SO3+H2O,Ⅲ中发生CaSO4+4C=CaS+4CO↑,
(1)二氧化硫与碳酸钙反应生成亚硫酸钙与二氧化碳,反应方程式为:SO2+CaCO3=CaSO3+CO2,亚硫酸钙在水存在的条件下被氧气氧化生成CaSO4•2H2O,反应方程式为:2CaSO3+O2+4H2O=2(CaSO4•2H2O),总反应为:2CaCO3+2SO2+O2+4H2O═2(CaSO4•2H2O)+2CO2;
S~SO2 ~CaSO4•2H2O
32 172
300t×2.5%×96% m
$\frac{32}{300t×2.5%×96%}=\frac{172}{m}$,解得m=38.7t,
故答案为:38.7.
(2)操作a是从亚硫酸铵溶液中获得亚硫酸铵晶体,亚硫酸铵晶体受热易分解,所以操作a为冷却结晶、过滤,
故答案为:冷却结晶、过滤;
(3)反应Ⅲ化学方程式为:CaSO4+4C=CaS+4CO↑,氧化剂为CaSO4,还原剂为C,反应中氧化剂与还原剂的物质的量之比为1:4,
故答案为:1:4;
(4)反应Ⅳ为NH4HCO3、CaSO4、NH3反应生成碳酸钙和硫酸铵,反应方程式为CaSO4+2NH3+CO2+H2O=(NH4)2SO4+CaCO3↓,操作b所得滤液中阳离子为铵根离子,其操作为取溶液少许加入NaOH并加热,生成有刺激性气味的气体能使湿润的红色石蕊试纸变蓝,
故答案为:CaSO4+2NH3+CO2+H2O=(NH4)2SO4+CaCO3↓;取溶液少许加入NaOH并加热,生成有刺激性气味的气体能使湿润的红色石蕊试纸变蓝;
(5)反应V中选用了40%的乙二醇溶液,温度控制在25℃,此时硫酸钾的产率超过90%,选用40%的乙二醇溶液原因是利用乙二醇降低硫酸钾溶解度,有利于析出,
故答案为:由于K2SO4在乙二醇溶液中的溶解度小,能够形成晶体而析出,因此符合复分解反应发生的条件;
(6)根据上面的分析可知,循环使用的物质为CaCO3,CO2,
故答案为:CaCO3,CO2.
点评 本题考查混合物分离提纯的综合应用,为高频考点,把握发生的反应、物质的性质、离子检验及原电池、氧化还原反应等为解答的关键,侧重分析与应用能力的考查,题目难度中等


科目:高中化学 来源: 题型:选择题
| A. | C (s)+O2(g)=CO (g)△H=-110.5 kJ/mol | |
| B. | C (s)+O 2(g)=CO2(g)△H=-393.5 kJ/mol | |
| C. | 2H2(g)+O2(g)=2H2O (l)△H=-571.6 kJ/mol | |
| D. | H2(g)+$\frac{1}{2}$O2(g)=H2O (g)△H=-241.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素编号 | 元素性质或原子结构 |
| T | 失去一个电子后,形成Ne原子电子层结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 其单质之一是空气中主要成分,最常见的助燃剂 |
| Z | 形成双原子单质分子,黄绿色气体 |
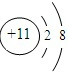 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
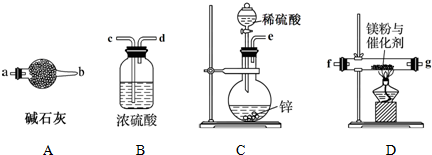
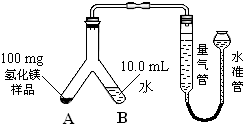
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 颜色 | 水溶性 | |
| 对氯甲苯 | 126.5 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
| 对氯苯甲酸 | 156.5 | 243 | 275 | 1.54 | 白色 | 微溶 |
| 对氯苯甲酸钾 | 194.5 | 具有盐的通性,属于可溶性盐 | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 甘氨酸(NH2CH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
| 易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有较强酸性和还原性 | 易溶于水,难溶于乙醇 |
| 实验 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 体系pH | 4.0 | 4.5 | 5.0 | 5.5 | 6.0 | 6.5 | 7.0 | 7.5 |
| 产率/% | 65.74 | 74.96 | 78.78 | 83.13 | 85.57 | 72.98 | 62.31 | 56.86 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,反应C(s)+CO2(g)?2CO(g)△H=a kJ/mol不能自发进行,则该反应的a<0 | |
| B. | 已知中和热△H为-57.3kJ/mol,则稀醋酸与0.1 mol/L NaOH溶液反应的热化学方程式为H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol | |
| C. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol,则氢气的燃烧热△H为-241.8 kJ/mol | |
| D. | 密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成17.6g硫化亚铁时,放出19.12kJ热量.该反应的热化学方程式可表示为Fe(s)+S(s)═FeS(s)△H=-95.6 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 空硬质玻璃管 | 硬质玻璃管+氧化铜 | 硬质玻璃管+铜 | |
| 质量(g) | w | m | n |
| A. | $\frac{16m}{m-n}$ | B. | $\frac{16(w-n)}{m-n}$ | C. | $\frac{16n}{m-n}$ | D. | $\frac{16(n-w)}{m-n}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com