
【题目】下列物质的沸点由高到低排列的是( )
①CH3(CH2)2CH3
②CH3(CH2)3CH3
③(CH3)3CH
④(CH3)2CHCH2CH3 .
A.②④①③
B.④②③①
C.④②①③
D.②④③①
科目:高中化学 来源: 题型:
【题目】下列关于乙酸性质的叙述中,错误的是
A. 乙酸的酸性比碳酸强,所以它可以与碳酸盐反应,产生CO2气体
B. 乙酸能与醇类物质发生酯化反应
C. 乙酸分子中含有碳氧双键,所以它能使溴水褪色
D. 乙酸在温度低于16.6 ℃时,就凝结成冰状晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:
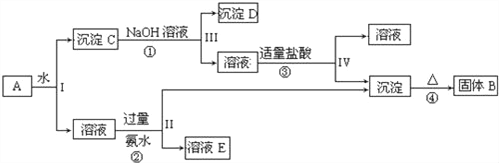
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是_____.
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式
沉淀固体B______;C________;沉淀D_____;溶液E________.
(3)写出①、②、③、④四个反应方程式
①_________________________;
②________________________;
③________________________;
④________________________.
【答案】 过滤 Al2O3 Al2O3、Fe2O3 Fe2O3 K2SO4、(NH4)2SO4 Al2O3+2NaOH+3H2O=2Na[Al(OH)4] 2KAl(SO4)2+6 NH3.H2O=K2SO4+3(NH4)2SO4+2Al(OH)3↓ Na[Al(OH)4]+HCl=NaCl+H2O+Al(OH)3↓ 2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
【解析】KAl(SO4)2溶于水,Al2O3和Fe2O3均不溶于水,混合物A加水溶解后,溶液中是KAl(SO4)2,沉淀C为Al2O3和Fe2O3;由转化关系图可知,向沉淀C中加NaOH溶液,Fe2O3不反应,沉淀D为Fe2O3,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,Al(OH)3受热分解生成固体B为Al2O3;向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中E为K2SO4、(NH4)2SO4,经过蒸发、结晶,得到K2SO4和(NH4)2SO4;
(1)溶液和沉淀的分离利用过滤;
(2)由上述分析可知B为Al2O3,C为Al2O3、Fe2O3,D为Fe2O3溶液E为K2SO4、(NH4)2SO4;
(3)反应①为Al2O3+2NaOH+3H2O=2Na[Al(OH)4],
反应②为2KAl(SO4)2+6NH3.H2O=K2SO4+3(NH4)2SO4+2Al(OH)3↓,
反应③为Na[Al(OH)4]+HCl=NaCl+H2O+Al(OH)3↓,
反应④为2Al(OH)3![]() Al2O3+3H2O。
Al2O3+3H2O。
点睛:考查无机物的推断,综合考查元素化合物性质,侧重Al、Fe及其化合物性质的考查,注意氧化铝的两性,明确发生的化学反应为解答的关键,由转化关系图可知,向沉淀C中加NaOH溶液,Fe2O3不反应,沉淀D为Fe2O3,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,Al(OH)3受热分解生成固体B为Al2O3;向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中E为K2SO4、(NH4)2SO4,经过蒸发、结晶,得到K2SO4和(NH4)2SO4,然后结合物质的性质及化学用语来解答。
【题型】填空题
【结束】
26
【题目】在常温下,Fe与水并不发生反应,但在高温下,Fe与水蒸气可发生反应。应用如图所示装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下Fe与水蒸气反应的实验。

请回答该实验中的问题。
(1)写出Fe与水蒸气反应的化学方程式:____________________________________。
(2)实验前必须对整套装置进行的操作是__________________________。
(3)圆底烧瓶中盛装的是水,该装置受热后的主要作用是_________________________。
(4)干燥管中盛装的物质可以是________________,作用是_______________。
(5)试管中收集到的气体,若要在处玻璃管口处点燃该气体,则必须对该气体进行__________,目的是:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数118,中子数为175的超重元素,该元素原子核内中子数与核外电子数之差是
A. 47B. 57C. 61D. 293
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一份含有杂质MgCl2和KCl的AlCl3溶液M,某小组用下图所示过程对其进行除杂并尽可能的减少AlCl3的损失。请回答下列问题:
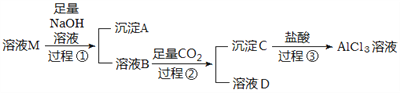
(1)沉淀A的化学式为__________,过程①中Al3+发生反应的离子方程式为__________________。
(2)氢氧化钠溶液_____(填“能”或“不能”)用氨水代替,原因是_____________________。
(3)溶液B中大量存在的阳离子是______________,过程②中生成沉淀C的离子方程式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】列说法中正确的是( )
A. 第ⅦA族中元素的最高化合价都是+7价
B. 第VA族元素的最高化合价一定是+6价
C. 第ⅣA族元素的最高化合价都是+4价
D. 第IA族中都是活泼的金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧印刷电路板的回收利用可实现资源再生,并减少污染.废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末.
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是(填字母).
A.热裂解形成燃油
B.露天焚烧
C.作为有机复合建筑材料的原料
D.直接填埋
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64.39kJmol﹣12H2O2(l)═2H2O(l)+O2(g)△H=﹣196.46kJmol﹣1
H2(g)+ ![]() O2(g)═H2O(l)△H=﹣285.84kJmol﹣1
O2(g)═H2O(l)△H=﹣285.84kJmol﹣1
在 H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为 .
(3)控制其他条件相同,印刷电路板的金属粉末用10%H2O2和3.0molL﹣1H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表).
温度(℃) | 220 | 330 | 440 | 550 | 660 | 770 | 880 |
铜平均溶解速率(×10﹣3molL﹣1min﹣1) | 77.34 | 88.01 | 99.25 | 77.98 | 77.24 | 66.73 | 55.76 |
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是 .
(4)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀.制备CuCl的离子方程式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com