
����Ŀ����ҵ�ϲ��û�ѧ�������������Ը�Ũ�Ⱥ����ˮ������Ҫ��������H3AsO3��ʽ���ڣ�,ͬʱ�ӳ����л�������ȡ�����õ���ҩҩ��As2O3������ʵ���˷�ˮ�������̵������������ŷš����������£�

�ش��������⣺
��1��H3AsO3�У���Ԫ�صĻ��ϼ�Ϊ__________
��2��H3AsO3����Ԫ��������һ���͵ڶ���������ͨ����ˮ�е�OH-���ʵ�ֵ�����������ֱ�ӵ����H+����һ�����뷽��ʽΪH3AsO3+H2O![]() [As(OH)4]-+H+����ڶ������뷽��ʽΪ________________________________��
[As(OH)4]-+H+����ڶ������뷽��ʽΪ________________________________��
��3����֪��As2S3�������S2-�������·�Ӧ��As2S3(s)+3S2-(aq) ![]() 2AsS33-(aq)�� ��һ����������FeSO4��������___________________________________________________
2AsS33-(aq)�� ��һ����������FeSO4��������___________________________________________________
��4��������������������A����Ҫ�ɷ֣�������Ca3(AsO4)2 ��FeAsO4��Fe(OH)3�⣬����________��д��ѧʽ����
��5��д���������У���Na3AsO4�Ʊ�As2O3 �����ӷ���ʽ ____________________________ ��
��6�����ᣨH3AsO4���ֲ������ƽ�ⳣ��(25��)Ϊ��K1=5.6��10��3 �� K2=1.7��10��7 �� K3=4.0��10��12�� Na3AsO4�ĵ�һ��ˮ������ӷ���ʽΪ��AsO43��+H2O![]() HAsO42��+OH�����ò�ˮ���ƽ�ⳣ����25����Ϊ__________��������λ��Ч���֣���
HAsO42��+OH�����ò�ˮ���ƽ�ⳣ����25����Ϊ__________��������λ��Ч���֣���
��7���ƻƣ�As2S3�����ۻ�(As4S4 )����Ȼ���г������黯�һ�������£����ߵ�ת����ϵ����ͼ��ʾ������Ӧ���У�1mol As4S4������AsԪ�صĻ��ϼ�Ϊ+2�ۣ��μӷ�Ӧʱ��ת��28mole-��������aΪ_________��

���𰸡�+3 [As(OH)4]-+H2O![]() [As(OH)5]2-+H+ ��������S2-��ʹƽ��As2S3(s)+3S2-(aq)
[As(OH)5]2-+H+ ��������S2-��ʹƽ��As2S3(s)+3S2-(aq) ![]() 2AsS33-(aq)��������߳���Ч�� CaSO4 2AsO43��+2SO2+2H+=As2O3+2SO42��+H2O 2.5��10��3 SO2
2AsS33-(aq)��������߳���Ч�� CaSO4 2AsO43��+2SO2+2H+=As2O3+2SO42��+H2O 2.5��10��3 SO2
��������
��1������H3AsO3�У����ϼ۴�����Ϊ0�Ĺ���ȷ����Ԫ�صĻ��ϼۣ�
��2�����һ���͵ڶ���������ͨ����ˮ�е�OH-���ʵ�ֵģ����ԱȽϵ�һ�����뷽��ʽ����д�ڶ�������ķ���ʽ��
��3����As2S3(s)+3S2-(aq) ![]() 2AsS33-(aq)�����淴Ӧ���֣�����FeSO4�����ã�
2AsS33-(aq)�����淴Ӧ���֣�����FeSO4�����ã�
��4�����������顱�Ǽ���H2O2��CaOʵ�ֵģ���ΪCaSO4�������ᣬ���Ի���CaSO4��
��5���������У���Na3AsO4�����������º�SO2��Ӧ�Ʊ�As2O3 �ģ�
��6������ˮ��ƽ�ⳣ����ʽ������K3������ˮ��ƽ�ⳣ����
��7������ͼʾ��ϵ���غ���ɣ����Ƴ�a��
��1������H3AsO3�У����ϼ۴�����Ϊ0�Ĺ���OΪ-2��HΪ+1����As�Ļ��ϼ�Ϊ+3��
�������+3��
��2���Աȵ�һ�����뷽��ʽ���ɵõڶ�������ĵ��뷽��ʽΪ��[As(OH)4]-+H2O![]() [As(OH)5]2-+H+
[As(OH)5]2-+H+
�������[As(OH)4]-+H2O![]() [As(OH)5]2-+H+��
[As(OH)5]2-+H+��
��3����ΪAs2S3�������S2-�������¿��淴Ӧ��As2S3(s)+3S2-(aq) ![]() 2AsS33-(aq)�����Լ���FeSO4����S2-����FeS(S)��ƽ���������ƶ�����߳���Ч����
2AsS33-(aq)�����Լ���FeSO4����S2-����FeS(S)��ƽ���������ƶ�����߳���Ч����
�����Ϊ����������S2-��ʹƽ��As2S3(s)+3S2-(aq) ![]() 2AsS33-(aq)���ƣ���߳���Ч����
2AsS33-(aq)���ƣ���߳���Ч����
��4�����������顱�Ǽ���H2O2��CaOʵ�ֵģ���ΪCaSO4�������ᣬ���Ի���CaSO4��
�������CaSO4��
��5���������У���Na3AsO4�����������º�SO2��Ӧ�Ʊ�As2O3 �ģ��������ӷ���ʽΪ��2AsO43��+2SO2+2H+=As2O3+2SO42��+H2O��
�������2AsO43��+2SO2+2H+=As2O3+2SO42��+H2O��
��6��ˮ������ӷ���ʽΪ��AsO43��+H2O![]() HAsO42��+OH�����ò�ˮ���ƽ�ⳣ��Kh=c(OH-)c(HAsO42��)/c(AsO43��)= c(OH-)c(HAsO42��)c(H+)/ c(AsO43��) c(H+)=Kw/K3=
HAsO42��+OH�����ò�ˮ���ƽ�ⳣ��Kh=c(OH-)c(HAsO42��)/c(AsO43��)= c(OH-)c(HAsO42��)c(H+)/ c(AsO43��) c(H+)=Kw/K3=![]() =2.5
=2.5![]() ��
��
�������2.5![]() ��
��
��7����ת����ϵͼ���Կ������˹�����As4S4��O2��Ӧ����AS2O3��a������ת��28mole-������7molO2�μӷ�Ӧ�����������غ㲻��д����Ӧ�Ļ�ѧ����ʽΪ��As4S4![]() 7O2=2 AS2O3
7O2=2 AS2O3![]() 4SO2����a��SO2��
4SO2����a��SO2��
�������SO2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�Ͽ��üױ��ϳɱ���ȩ��
 ��
��
����˵����ȷ����
A. �ױ�����������ԭ�Ӷ���ͬһƽ���� B. ��Ӧ�٢ڢ۵ķ�Ӧ������ͬ
C. һ�ȼױ���ͬ���칹����3�� D. ���״���������Ʒ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦFe+H2SO4=FeSO4+H2���������仯���ƣ���ͼ��ʾ��

(1)�÷�ӦΪ____��Ӧ��������������������������
(2)��Ҫʹ�÷�Ӧ�ķ�Ӧ���ʼӿ죬���д�ʩ���е���____������ĸ����
A.����ƬΪ���� B.�μ�����CuSO4 ��Һ
C.�����¶� D.��ϡ�����Ϊ98%��Ũ����
(3)����������Ӧ��Ƴ�ԭ��أ�ͭΪԭ���ijһ�����ϣ���ͭΪ_______������������������������ͭƬ�ϲ���������Ϊ________���ü��Ϸ����ĵ缫��ӦΪ_______��2min����Ƭ����������1.4 g�������������ĵ���Ϊ____mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Դ�����ǵ����������������չ���ش�����֮һ����������ת������ȷ����
A.��¯ȡů�ǽ�����ת��Ϊ����
B.�ƾ�ȼ���ǽ���ѧ��ת������
C.̫���ܷ����ǽ���ѧ��ת��Ϊ����
D.�ֻ�����ǽ�����ת��Ϊ��ѧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ������ȷ����
A. HSO3��+ H2O![]() SO32�� + OH�� B. Al3+ + 3H2O == 3H+ + Al��OH��3��
SO32�� + OH�� B. Al3+ + 3H2O == 3H+ + Al��OH��3��
C. NaHCO3 == Na+ + HCO3�� D. H2S![]() 2H+ + S2��
2H+ + S2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�о����������ɼ���ת����ijС���������ʵ�顣���ڸ�ʵ�����������ȷ����
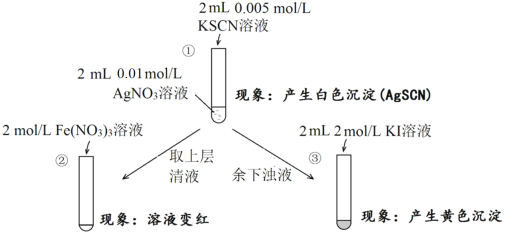
A������Һ�д���ƽ�⣺AgSCN(s)![]() Ag+(aq)+SCN-(aq)
Ag+(aq)+SCN-(aq)
B��������ɫ�仯˵���ϲ���Һ�к���SCN-
C��������ɫ�仯˵����AgI����
D����ʵ�����֤��AgI��AgSCN������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йع�Ͷ����������;�������(����)
A.�赥�����ͻ����B.��������뵼�����
C.�������������ά����D.�ߴ����������оƬ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���X�Ľṹ��ʽ��ͼ��ʾ�������й�˵������ȷ����
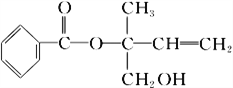
A. X�����к������ֹ�����
B. �������Ը��������Һ���𱽺�X
C. X��һ���������ܷ����ӳɡ��Ӿۡ�ȡ���������ȷ�Ӧ
D. �ڴ����������£�1 mol X�������5 mol H2�ӳ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ʼ��仯�����ڹ�ҵ���й㷺Ӧ�ã�
(1)ͬ��ʯ�ڸ������Ʊ������Ȼ�ѧ����ʽΪ��
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)�T3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)��H
��֪��ͬ�����£�
4Ca3(PO4)2F(s)+3SiO2(s)�T6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)��H1
2Ca3(PO4)2(s)+10C(s)�TP4(g)+6CaO(s)+10CO(g)��H2
SiO2(s)+CaO(s)�TCaSiO3(s)��H3
�á�H1����H2�͡�H3��ʾ��H�����H=______��
(2)�����������Ϊ�����������(����ṹʽ��ͼ)֮����ȥ����ˮ���Ӳ����ṹʽΪ______������������(�׳���������)�dz��õ�ˮ���������仯ѧʽΪ______��

(3)��������(NaH2PO2)�����ڹ�ҵ�ϵĻ�ѧ������
�ٻ�ѧ��������Һ�к���Ni2+��H2PO2���������Ե������·���������Ӧ��
(a)������������Ni2++������������H2PO2��+��������������������������Ni++������������H2PO3��+������������
(b)6H2PO��2+2H+�T2P+4H2PO3+3H2��
���ڴ����д������ƽ��Ӧʽ(a) ___________________________��
�����â��з�Ӧ�������϶Ƽ�������������Ͻ𣬴Ӷ��ﵽ��ѧ������Ŀ�ģ�����һ�ֳ����Ļ�ѧ�ƣ�������·���Ƚϻ�ѧ�����ƣ�
�����ϵIJ�ͬ�㣺______��
ԭ���ϵIJ�ͬ�㣺______��
��ѧ�Ƶ��ŵ㣺______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com