
| A. | 16g | B. | 8g | C. | 40g | D. | 0.2mol |
分析 向所得溶液中加入NaOH溶液至Mg2+恰好完全沉淀,沉淀为Mg(OH)2,沉淀过滤洗涤灼烧至质量不再变化,最终得到MgO,生成NO2、N2O4、NO 的混合气体与2.24L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,纵观整个过程,由电子转移守恒,可知Mg提供电子等于氧气获得的电子,再根据Mg原子守恒计算MgO物质的量,根据m=nM计算其质量.
解答 解:向所得溶液中加入NaOH溶液至Mg2+恰好完全沉淀,沉淀为Mg(OH)2,沉淀过滤洗涤灼烧至质量不再变化,最终得到MgO,生成NO2、N2O4、NO 的混合气体与2.24L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,纵观整个过程,由电子转移守恒,可知Mg提供电子等于氧气获得的电子,氧气获得电子为:$\frac{2.24L}{22.4L/mol}$×4=0.4mol,故Mg的物质的量为$\frac{0.4mol}{2}$=0.2mol,根据Mg原子守恒,可知MgO物质的量为0.2mol,故MgO质量为0.2mol×40g/mol=8g,故选BD.
点评 本题考查混合物计算,难度中等,侧重考查学生的分析思维能力与解题方法技巧,注意利用守恒法进行解答.


科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Cl->Mg2+>Na+ | B. | 热稳定性:HF>H2O>H2S | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 非金属性:Cl>Br>I |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
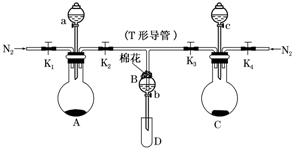 某实验小组用如图所示装置进行实验以探究Fe3+、Cl2和SO2的氧化性强弱(夹持仪器已略).
某实验小组用如图所示装置进行实验以探究Fe3+、Cl2和SO2的氧化性强弱(夹持仪器已略).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的比例模型是: | B. | 二氧化碳的电子式: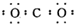 | ||
| C. | CO2的比例模型: | D. | HClO的结构式为:H-O-Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
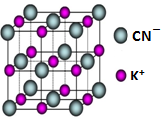 目前工业上制备丙烯腈(CH2=CHC≡N)有乙炔法、丙烯氨氧化法等.
目前工业上制备丙烯腈(CH2=CHC≡N)有乙炔法、丙烯氨氧化法等.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com