
| A. | pH<7的雨水 | B. | pH<5.6的雨水 | C. | pH=5.6的雨水 | D. | pH>7的雨水 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
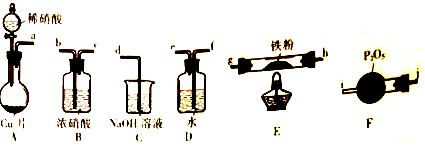
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=-121.5kJ•mol-1 | |
| B. | 2CO2(g)+3H2(g)═$\frac{1}{2}$CH3OCH3(g)+$\frac{3}{2}$H2O(g)△H=-25.5kJ•mol-1 | |
| C. | 2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=+121.5kJ•mol-1 | |
| D. | 2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=-72.5kJ•mol-1. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
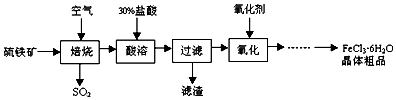
| A. | “焙烧”反应中,氧化产物是SO2,还原产物是Fe3O4 | |
| B. | “酸溶”时的酸可以用稀硫酸代替 | |
| C. | “过滤“后的滤液中Fe3+和Fe2+的浓度比为2:1 | |
| D. | “氧化”时的氧化剂只能选取Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 分类标准 | 金属单质 | 碱性氧化物 | 硝酸盐 | 非电解质 |
| 属于该类的物质(填序号) | ② | ③ | ⑥ | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能在水溶液或熔融状态下导电的物质是电解质 | |
| B. | 电离出氢离子的化合物是酸 | |
| C. | 氧化还原反应中转移电子数等于得电子数与失电子数加和 | |
| D. | 丁达尔效应可用来区别溶液和胶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com