
| A. | 电解质与非电解质的本质区别:是在水溶液或熔化状态下能否电离 | |
| B. | 强电解质与弱电解质的本质区别:其水溶液导电性的强弱 | |
| C. | 胶体与溶液的本质区别:是否有丁达尔现象 | |
| D. | 氧化还原反应的本质:元素化合价在反应前后发生改变 |
分析 A.在水溶液或熔化状态下能够发生电离的化合物是电解质,在水溶液和熔化状态下均不能发生电离的化合物是非电解质;
B.在水溶液或熔融状态下完全电离出离子的电解质是强电解质,在水溶液或熔融状态下部分电离出离子的电解质是弱电解质;
C.根据分散质粒子直径不同把分散系分为溶液、胶体、浊液;
D.氧化还原反应的本质是电子的转移.
解答 解:A.在水溶液或熔化状态下能够发生电离的化合物是电解质,在水溶液和熔化状态下均不能发生电离的化合物是非电解质,因此电解质与非电解质的本质区别:是在水溶液或熔化状态下能否电离,故A正确;
B.在水溶液或熔融状态下完全电离出离子的电解质是强电解质,在水溶液或熔融状态下部分电离出离子的电解质是弱电解质,因此强电解质与弱电解质的本质区别是在水溶液或熔融状态下的电离程度,故B错误;
C.胶体与溶液的本质区别是分散质粒子直径不同,故C错误;
D.氧化还原反应的本质是电子的转移,氧化还原反应的特征是元素化合价在反应前后发生改变,故D错误;
故选:A.
点评 本题考查化学基本概念的辨析,难度不大,掌握电解质与非电解质、强电解质与弱电解质、分散系以及氧化还原反应等概念是解题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | X的最高正化合价为6 | B. | X是金属元素 | ||
| C. | X位于第7周期第ⅥA族 | D. | X为非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| B. | 电解熔融MgCl2,可制得金属镁 | |
| C. | 在铁制品上镀银时,镀件为阳极,银盐为电镀液 | |
| D. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | υ(A)=0.5 mol/(L•s) | B. | υ(B)=0.3 mol/(L•s) | C. | υ(C)=12 mol/(L•min) | D. | υ(D)=6 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冷的浓硫酸和浓硝酸都不可以用铝、铁的容器盛装 | |
| B. | 所有铵盐都易溶于水,所有铵盐中的氮均呈-3价 | |
| C. | 由于铵盐易和碱反应生成氨气,所以在实验室中一般用NH4Cl和NaOH的混合物制取氨气 | |
| D. | 金和铂不溶于浓硫酸和浓硝酸,但能溶于王水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾溶液加热 | B. | CH3COONa溶液加热 | ||
| C. | 氨水中加入少量NH4Cl | D. | Na2CO3溶液中加入BaCl2固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①②③④ | C. | ②③④⑥ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧气 | B. | 氮气 | C. | C2H4 | D. | NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
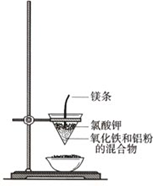 铁和铝是两种重要的金属.请回答:
铁和铝是两种重要的金属.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com