
 根据硫化氢气体的实验室制法和性质完成下列填空。
根据硫化氢气体的实验室制法和性质完成下列填空。
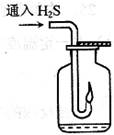
 若用启普发生器制取硫化氢气体,则制取气体的原料可选用________。
若用启普发生器制取硫化氢气体,则制取气体的原料可选用________。 a.稀硫酸与硫化亚铁 b.稀硝酸与硫化亚铁
a.稀硫酸与硫化亚铁 b.稀硝酸与硫化亚铁 c.稀硫酸与硫化钠 d.稀盐酸与硫化亚铁
c.稀硫酸与硫化钠 d.稀盐酸与硫化亚铁 小题2:现要组装一套可以控制硫化氢气体产生速率的装置,请在下图中选择合适的仪器;
小题2:现要组装一套可以控制硫化氢气体产生速率的装置,请在下图中选择合适的仪器; ______________(填编号)。
______________(填编号)。




 小题3:如右图,在一个充满氧气的集气瓶中加入少量品红稀硫溶液,
小题3:如右图,在一个充满氧气的集气瓶中加入少量品红稀硫溶液, 点燃硫化氢气体。在火焰自动熄灭后,停止通入气体,瓶内可观察到
点燃硫化氢气体。在火焰自动熄灭后,停止通入气体,瓶内可观察到 的现象是___________________________________________________。
的现象是___________________________________________________。 小题4:在上述集气瓶中继续通入硫化氢气体,振荡,发生反应的化学方程式为:
小题4:在上述集气瓶中继续通入硫化氢气体,振荡,发生反应的化学方程式为: ______________________________________________________________
______________________________________________________________ 反应过程中,溶液的pH______(填“变大”、“变小”或“不变”)。
反应过程中,溶液的pH______(填“变大”、“变小”或“不变”)。 小题5:点燃不纯的硫化氢气体可能会发生爆炸,为了防止意外,可连接一个安全装置。下图的装置能起到此作用的是___________。
小题5:点燃不纯的硫化氢气体可能会发生爆炸,为了防止意外,可连接一个安全装置。下图的装置能起到此作用的是___________。

 小题6:已知硫化氢气体在空气中的体积分数为4.3%~45.5%时会发生爆炸。当硫化氢气体在空气中的体积分数为30%时,其爆炸产物是______________________。
小题6:已知硫化氢气体在空气中的体积分数为4.3%~45.5%时会发生爆炸。当硫化氢气体在空气中的体积分数为30%时,其爆炸产物是______________________。 小题1:a d
小题1:a d  小题2:② ③ ④
小题2:② ③ ④ 小题3:品红溶液褪色;瓶壁有淡黄色粉末和无色的小液滴
小题3:品红溶液褪色;瓶壁有淡黄色粉末和无色的小液滴 小题4:
小题4: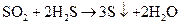 变大
变大 小题5:b
小题5:b 小题6:S H2O
小题6:S H2O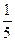 =14%,O2不足,发生反应2H2S+O2
=14%,O2不足,发生反应2H2S+O2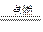 2S+2H2O。
2S+2H2O。

科目:高中化学 来源:不详 题型:填空题
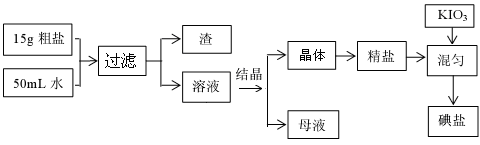
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
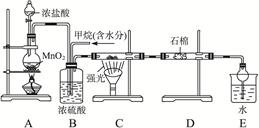 ?
?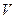 (Cl2)/
(Cl2)/ 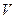 (CH4) =
(CH4) =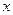 ,若理论上欲获得最多的氯化氢,则
,若理论上欲获得最多的氯化氢,则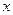 值的取值范围为___________。?
值的取值范围为___________。?查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 气体 | a | b | c | d |
| C2H4 | 乙醇 | 浓H2SO4 | NaOH溶液 | 浓H2SO4 |
| Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓H2SO4 |
| NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 固体NaOH |
| NO | 稀HNO3 | 铜屑 | H2O | P2O5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.可用过滤的方法除去氢氧化铁胶体中少量的氯化铁 |
| B.用酸式滴定管量取18.80mL的碳酸钠溶液 |
| C.配制0.1mol/L的硫酸时,用量筒量取浓硫酸,要洗涤量筒,否则配制的溶液浓度偏低 |
| D.振荡用饱和的碳酸钠溶液吸收乙酸乙酯的试管,发现有气泡冒出,它是CO2气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
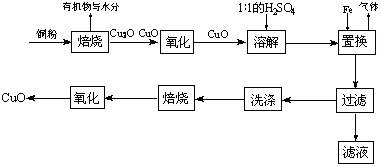
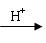 Cu+Cu2+)。请你设计一个简单的实验检验焙烧后固体(假设只含铜的氧化物)中是否含有Cu2O。
Cu+Cu2+)。请你设计一个简单的实验检验焙烧后固体(假设只含铜的氧化物)中是否含有Cu2O。 查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
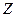 。
。
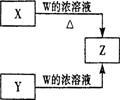
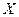 是黑色粉末,
是黑色粉末,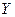 是白色固体(焰色反应透过蓝色钴玻璃呈紫色,可用于制备火柴),且都是常见的氧化剂。
是白色固体(焰色反应透过蓝色钴玻璃呈紫色,可用于制备火柴),且都是常见的氧化剂。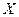 与W的浓溶液共热生成
与W的浓溶液共热生成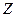 的离子方程式 。
的离子方程式 。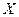 与
与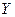 混合后共热可产生一种无毒气体,反应的化学方程式为 。
混合后共热可产生一种无毒气体,反应的化学方程式为 。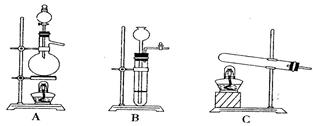
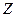 与乙烯加成可得一种有机物,为验证该有机物中含有与
与乙烯加成可得一种有机物,为验证该有机物中含有与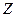 相同的元素,请选择合适的试剂 (用字母编号回答)。
相同的元素,请选择合适的试剂 (用字母编号回答)。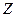 时,通常可用排某种溶液的方法收集
时,通常可用排某种溶液的方法收集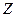 ,则该溶液是 ;也可用排空气集气法收集
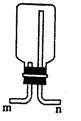
,则该溶液是 ;也可用排空气集气法收集 ,若用右图装置(不能改变瓶口朝向),则气体应该从 (填“m”或“n”)口进。
,若用右图装置(不能改变瓶口朝向),则气体应该从 (填“m”或“n”)口进。 和氢气制备一种重要的化工原料,同时获取电能。假设这种想法可行,用石墨作电极材料,用稀盐酸作电解质溶液,则通入
和氢气制备一种重要的化工原料,同时获取电能。假设这种想法可行,用石墨作电极材料,用稀盐酸作电解质溶液,则通入 的电极为原电池的 极,其电极反应式为 。
的电极为原电池的 极,其电极反应式为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
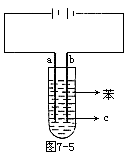
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com