
 ��
�� ���� ��1�����Ӳ�һ���࣬�˵����Խ�뾶ԽС���⻯�ƣ�CaH2����ˮ��Ӧ�����������������غ㶨�ɣ���Ӧǰ��Ԫ������䣬���������������ƣ�д����Ӧ�Ļ�ѧ����ʽ���ɣ�
��2��ͬ����Ԫ�صķǽ�����Խǿ����Ӧ�ĵ��ʵ�������Խǿ���⻯��Ļ�ԭ��Խ����
��3���縺��Խ�õ�������Խǿ������Ԫ����ʾ���ۣ����ݼ�����ˮѸ��ˮ������SiO2•nH2O������������д����ʽ�����ϼ�����Ԫ�ر��ֻ�ԭ�ԣ��������ڿ�����ȼ������B2O3��ˮ��
��4�����⻯�ƣ�NaBH4�����л���ѧ�е�һ�ֳ��û�ԭ��������ˮ��ˮ�����������ƺ��������ݴ���д����ʽ��
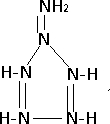
��5����״������ף�N6H6������Ϊ���ܲ��ϵĿ����ԣ���������3�ֻ�ѧ������Nԭ�Ӻ�2�ֻ�ѧ������Hԭ�ӣ���Nԭ�Ӿ��ﵽ8���ӽṹ����ԭ����Χ�γ��ĸ����ۼ����ݴ�д���ṹʽ��
��� �⣺��1��LiH��Li+��H-�ĵ��Ӳ���һ���࣬���Ӳ�һ���࣬�˵����Խ�뾶ԽС���ʰ뾶��Li+��H-���⻯�ƣ�CaH2����ˮ��Ӧ�����������������غ㶨�ɣ���Ӧǰ��Ԫ������䣬���������������ƣ���Ӧ�Ļ�ѧ����ʽΪ��CaH2+2H2O=Ca��OH��2+2H2����
�ʴ�Ϊ��С�ڣ�CaH2+2H2O=Ca��OH��2+2H2����
��2��ͬ����Ԫ�صķǽ�����Խǿ����Ӧ�ĵ��ʵ�������Խǿ���⻯��Ļ�ԭ��Խ�����������ڵ���̬�⻯������ȶ�����ǿ������˳��Ϊ��HCl��H2S��PH3��SiH4���ʴ�Ϊ��HCl��H2S��PH3��SiH4��
��3��H�ĵ縺��Խ�õ�������Խǿ��HԪ����ʾ���ۣ�����H��ʾ-1�ۣ�������ˮѸ��ˮ������SiO2•nH2O������ʽΪ��SiH4+��n+2��H2O=SiO2•nH2O+3H2�����������ڿ�����ȼ������B2O3��ˮ����Ӧ����ʽΪ��B2H6+3O2$\frac{\underline{\;��ȼ\;}}{\;}$B2O3+3H2O��BԪ�ػ��ϼ�����-3���ߵ�+3��BԪ�ر��ֻ�ԭ�ԣ��������ǿ��ԭ��������B��
�ʴ�Ϊ��-1��SiH4+��n+2��H2O=SiO2•nH2O+3H2����B��
��4�����⻯�ƣ�NaBH4�����л���ѧ�е�һ�ֳ��û�ԭ��������ˮ��ˮ�����������ƺ���������Ӧ����ʽΪ��NaBH4+4H2O�TNa[B��OH��4]+4H2����NaBH4+2H2O�TNaBO2+4H2�����ʴ�Ϊ��NaBH4+4H2O�TNa[B��OH��4]+4H2����NaBH4+2H2O�TNaBO2+4H2����
��5����������3�ֻ�ѧ������Nԭ�Ӻ�2�ֻ�ѧ������Hԭ�ӣ���Nԭ�Ӿ��ﵽ8���ӽṹ����ԭ����Χ�γ��ĸ����ۼ����ݴ�д���ṹʽ����Ϊ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼��������ˮ�⡢���뾶�Ƚϡ����ʽṹ��������ѧ����ʽ�����ӷ���ʽ��д�����ڱ��еݱ���ɵ�֪ʶ�㣬���ջ����ǽ���ؼ�����Ŀ�ѶȽϴ�


 �¿α�������������ҵ�������γ�����ϵ�д�
�¿α�������������ҵ�������γ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
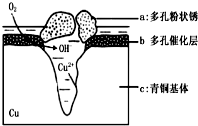 ��ͭ�����������л������Ͷ������ǻ۵Ľᾧ����Ϊһ��ʱ��������������������ͭ������ܵ�������ʴ����ͼΪ��ͭ���ڳ�ʪ�����з����绯ѧ��ʴ��ԭ��ʾ��ͼ�������е� Cl- ��ɢ���ڣ�������缫�����������ɶ��״�� Cu2 �� OH ��3 Cl������˵������ȷ���ǣ�������
��ͭ�����������л������Ͷ������ǻ۵Ľᾧ����Ϊһ��ʱ��������������������ͭ������ܵ�������ʴ����ͼΪ��ͭ���ڳ�ʪ�����з����绯ѧ��ʴ��ԭ��ʾ��ͼ�������е� Cl- ��ɢ���ڣ�������缫�����������ɶ��״�� Cu2 �� OH ��3 Cl������˵������ȷ���ǣ�������| A�� | ��ʴ�����У����� b ������ | |
| B�� | �����е�Cl-��ɢ���ڣ�����������Ӧ���������Ӧ�����������ɶ��״��Cu2��OH��3Cl�������ӷ���ʽΪ2Cu2++3OH-+Cl-=Cu2��OH��3Cl�� | |
| C�� | ������ 2.145gCu 2 �� OH �� 3 Cl�������������ı�״���������Ϊ 0.448L | |
| D�� | �����ĵ缫��ӦʽΪ��������Ӧ�� O2+4e-+2H2O=4OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ȼ�ѧ����ʽ��֪d��c | |
| B�� | H2��ȼ����Ϊd kJ/mol | |
| C�� | CH3OH��g���TCO��g��+2H2��g����H=��b+2c-a��kJ/mol | |
| D�� | ��CO��H2�����ʵ���֮��Ϊ1��2ʱ������ȫȼ������CO2��H2O��l��ʱ���ų�Q kJ��������������CO�����ʵ���Ϊ$\frac{Q}{b+2c}$mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij�о���ѧϰС����PH=1������ζ�25.00mLδ֪���ʵ���Ũ�ȵ�NaOH��Һ���Ӷ������NaOH��Һ��PHֵ��ѡ�÷�̪��Ϊָʾ����
ij�о���ѧϰС����PH=1������ζ�25.00mLδ֪���ʵ���Ũ�ȵ�NaOH��Һ���Ӷ������NaOH��Һ��PHֵ��ѡ�÷�̪��Ϊָʾ����| �ζ����� | ����Һ�����mL�� | �����������mL�� | |
| �ζ�ǰ������mL�� | �ζ��������mL�� | ||
| ��һ�� | 25.00 | 0.50 | 20.40 |
| �ڶ��� | 25.00 | 4.00 | 24.10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ȼ�� | B�� | ���ȼ� | C�� | ���� | D�� | ��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2 LŨ��Ϊ0.5 mol/L ������Һ�к���NA�������� | |
| B�� | 1molFeCl3���ˮ��Ӧ����NA��Fe��OH��3���� | |
| C�� | ��14g CO�к��е�ԭ����ΪNA | |
| D�� | ��H2O2+Cl2�T2HCl+O2��Ӧ�У�ÿ����32 g������ת�Ƶ�����4 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  H2S���ռ� | B�� |  NO���ռ� | C�� | 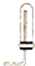 NH3���ռ� | D�� |  Cl2���ռ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com