
| A、Na→NaOH→Na2CO3→NaCl |
| B、Al→Al2O3→Al(OH)3→AlCl3 |
| C、Mg→MgCl2→Mg(OH)2→MgSO4 |
| D、Fe→FeCl2→Fe(OH)2→Fe(OH)3 |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
| A、室温下,21.0g乙烯和丁烯的混合气体中含有的氢原子数目为1.5NA |
| B、标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2 NA |
| C、50℃时,pH=1的1.0L H2SO4溶液中含有的H+数目为0.1 NA |
| D、3.4g NH3中含N-H键数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
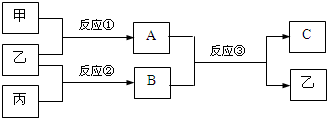 现有甲、乙、丙、A、B、C六种物质,其中甲、乙、丙是由短周期元素组成的单质.一定条件下转化关系如图所示:
现有甲、乙、丙、A、B、C六种物质,其中甲、乙、丙是由短周期元素组成的单质.一定条件下转化关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
 常温下,用 0.1mol?L-1HCl溶液滴定10.0mL浓度为0.1mol?L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,用 0.1mol?L-1HCl溶液滴定10.0mL浓度为0.1mol?L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )| A、当V=0时:c(H+)+c(HCO3-)+c(H2CO3)=c(OH-) |
| B、当V=5时:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Cl-) |
| C、当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| D、当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属镁与稀盐酸反应:有气泡逸出:Mg+2H++2Cl-═MgCl2+H2↑ |
| B、氯化钡溶液与稀硫酸反应:有白色沉淀生成:Ba2++SO42-═BaSO4↓ |
| C、碳酸钠与盐酸反应:有气泡逸出:Na2CO3+2H+═CO2↑+H2O+2Na+ |
| D、硫酸铜溶液中加入过量的NaOH溶液:有白色沉淀产生:Cu2++2OH-═Cu(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol Cl2完全溶于水,转移的电子数目为0.1NA |
| B、足量的硫单质与64g铜完全反应,转移电子数目为NA |
| C、1 mol Fe与足量的稀HNO3反应,转移2NA个电子 |
| D、含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,该反应的平衡常数K=0.2 |
| B、往平衡体系中加入金属铅后,c(Pb2+)增大 |
| C、往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变大 |
| D、升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com