
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②③⑤ |
分析 ①化合物是不同元素组成的纯净物,液氯是单质;
②依据混合物是不同物质组成的分析;
③电解质是水溶液中或熔融状态下导电的化合物;
④胶体的本质特征是分散质微粒直径在1nm-100nm间;
⑤过氧化钠是氧化物.
解答 解:①液氯是单质,干冰、磁性氧化铁均为化合物,故①错误;
②盐酸是氯化氢水溶液、水玻璃是硅酸钠水溶液、氢氟酸为混合物,故②正确;
③明矾、小苏打、纯碱,符合电解质概念,均为电解质,故③正确;
④碘酒是碘单质的酒精溶液、牛奶、豆浆是胶体,漂粉精为次氯酸盐的水溶液,故④错误;
⑤过氧化钠是氧化物,不是盐,故⑤错误
综上所述:②③正确;
故选B.
点评 本题考查了化学基本概念的理解和应用,熟悉混合物、化合物、单质、化合物、电解质、非电解质等概念的分析即可判断,掌握物质的组成是解题关键.


科目:高中化学 来源: 题型:解答题
 (1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度.则100℃时1mol•L-1的NaOH溶液中,由水电离出的c(H+)=1×10-12mol•L-1.25℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是促进(填“促进”、“抑制”或“不影响”).
(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度.则100℃时1mol•L-1的NaOH溶液中,由水电离出的c(H+)=1×10-12mol•L-1.25℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是促进(填“促进”、“抑制”或“不影响”).| 化学式 | 电离平衡常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正、逆反应速率都等于零 | B. | CO、H2S、COS、H2的浓度相等 | ||
| C. | CO、H2S、COS、H2在容器中共存 | D. | CO、H2S、COS、H2的浓度均不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
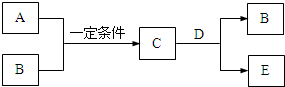 A、B、C、D、E是中学化学中的常见物质,A、B是短周期元素组成的单质.其转化关系如图:
A、B、C、D、E是中学化学中的常见物质,A、B是短周期元素组成的单质.其转化关系如图:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 做焰色反应实验时,应用H2SO4清洗铂丝 | |
| B. | 焰色反应是单质特有的性质 | |
| C. | 碳酸钾在酒精灯上灼烧时能直接观察到紫色火焰 | |
| D. | NaCl与Na2SO4灼烧时火焰颜色均为黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
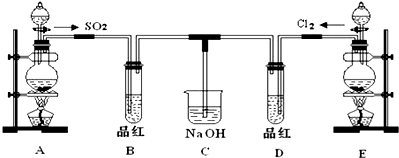
 ;请指出该反应中的液体反应物在反应中所表现出的化学性质:还原性和酸性;若液体中的溶质反应了6mol,则转移的电子的物质的量3mol;
;请指出该反应中的液体反应物在反应中所表现出的化学性质:还原性和酸性;若液体中的溶质反应了6mol,则转移的电子的物质的量3mol;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该分子中存在肽键 | |
| B. | 最多可以有12个碳原子共平面 | |
| C. | 1 mol氯雷他定最多可与8 mol氢气发生加成反应 | |
| D. | 能与NaOH溶液反应,但不能与NaHCO3溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com