
【题目】t℃时,向xgKNO3不饱和溶液中,加入agKNO3或蒸发掉bg水恢复到t℃,溶液均达到饱和,据此下列推论错误的是
A. 在t℃时,KNO3的溶解度为100a/b g
B. 若原溶液中溶质质量分数为![]() ,则x=2b
,则x=2b
C. 若原不饱和溶液蒸发掉2b g水,恢复到原温度,能析出2a gKNO3
D. 在t℃时所配得的KNO3溶液中溶质质量分数≤![]()
【答案】C
【解析】
A、将原不饱和溶液蒸发掉bg水之后可以达到饱和,在原溶液中加入ag溶质也可以达到饱和,说明ag溶质溶于bg水中恰好形成饱和溶液,可求出溶解度为 100a/b g,故A不符合题意;
B、根据溶解度的定义,在加入了ag溶质之后形成饱和溶液,可以列出式子:x× ![]() +a=(x+a)× (硝酸钾的溶解度÷硝酸钾的溶解度+100g),此处硝酸钾的溶解度可用100a/b g代替,可以解出x=2b,故B不符合题意;
+a=(x+a)× (硝酸钾的溶解度÷硝酸钾的溶解度+100g),此处硝酸钾的溶解度可用100a/b g代替,可以解出x=2b,故B不符合题意;
C、原不饱和溶液蒸发掉2bg水,蒸发掉bg水的时候刚好形成饱和溶液,此时继续蒸发掉bg水,析出溶质的质量就是溶解于bg水中的溶质的质量,为ag,故C符合题意;
D、在t℃时饱和硝酸钾溶液中溶质的质量分数为 ![]() ,配成的溶液质量分数应该小于等于饱和溶液中溶质的质量分数,故D不符合题意;
,配成的溶液质量分数应该小于等于饱和溶液中溶质的质量分数,故D不符合题意;
综上所述,本题应选C。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】绿色能源是指使用过程中不排放或排放极少污染物的能源,如一次能源中的水能、地热能、天然气等;二次能源中的电能、氢能等。下列能源属于绿色能源的是
①太阳能②风能③石油④煤⑤潮汐能⑥木材
A.①②③B.③④⑤C.④⑤⑥D.①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用粗盐(含Ca2+、Mg2+、SO42-等杂质)为主要原料采用“侯氏制城法”生产纯碱和化肥NH4Cl.工艺流程如图所示。下列有关说法不正确的是

A. 对粗盐溶液除杂可依次加入NaOH、Na2CO3、BaCl2,再加入盐酸调节溶液pH
B. 粗盐可采用除杂和重结晶等过程提纯
C. 流程图中的系列操作中用到的玻璃仪器可能有玻璃棒、烧杯、漏斗、坩埚等
D. 该流程中得到的晶体用到了溶解度的差异性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:C2H5OH+NaBr+H2SO4(浓) ![]() NaHSO4+C2H5Br+H2O,实验室用如图所示装置制备溴乙烷(沸点为38.4 ℃,密度为1.43 g·mL-l)。
NaHSO4+C2H5Br+H2O,实验室用如图所示装置制备溴乙烷(沸点为38.4 ℃,密度为1.43 g·mL-l)。

实验前先向仪器a 中加入10 g 乙醇和足量浓硫酸,然后加入研细的20.6g 溴化钠和几粒碎瓷片,向试管d中加人少量蒸馏水。
回答下列问题:
(1)加入碎瓷片的作用是__________________________。
(2)为了更好的控制反应温度,除用图示的加热方法外,更好的加热方法是_______________________。
(3)试管d 中出现的实验现象是__________________________。
(4)反应结束后,试管d中含少量杂质Br2,为了除去粗产品中的杂质Br2,可选用的试剂是________(填字母)
A.苯 B.H2O C.Na2SO3溶液 D.CCl4
(5)经过分离、提纯、干燥后,该实验最终得到8.7g溴乙烷,则本实验溴乙烷的产率为__________。
(6)通过以下几项实验步骤可检验溴乙烷中的溴元素,其正确的操作顺序是取少量溴乙烷,__________(填序号)。
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液 ⑤冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素X、Y、Z、T、W,原子序数依次增大。X的核外电子总数与其周期数相同,Y基态原子的p电子数比s电子数少1个,Z基态原子的价电子层中有2个未成对电子,T与Z同主族,W基态原子的M层全充满,N层只有一个电子。回答下列问题:
(1)Y、Z、T中单质熔点最高是______(填元素符号)
(2)比W原子序数少5的基态原子中单电子数为_________________。
(3)T与Z形成的化合物中,中心原子杂化类型是_______
(4)X和上述其他元素中的一种形成的化合物中:分子呈三角锥形的是________(填化学式);分子中既含有极性共价键,又含有非极性共价键的化合物是_______(填化学式,写一种)。
(5)这5种元素形成的一种阴阳离子个数比为1:1型的配合物中,阴离子呈四面体结构,阳离子的结构如图所示。该配合物的化学式为__________,阳离子中存在的化学键类型有_______。
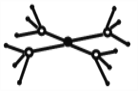
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F都是元素周期表中前36号元素,它们的原子序数依次增大。A原子基态时最外层电子数是其内层电子总数的2倍,C原子基态时s电子数与p电子数相等,D在元素周期表的各元素中电负性最大,E的基态原子核外有6个能级且全部充满电子,F原子基态时未成对电子数是同周期元素中最多的。
(1)F元素的名称是________ ,基态F原子的价电子轨道表示式_________画出AC2的电子式_______________E元素常见离子的电子排布式______________。
(2)A、B、C的电负性大小顺序(填元素符号,下同)______________,第一电离能大小顺序为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧熔融碳酸盐燃料电池是一种高温电池(600~700℃),具有效率高、噪音低、无污染、燃料多样、余热利用价值高等优点。氢氧熔融碳酸盐燃料电池的工作原理如图所示。下列有关该电池的说法正确的是
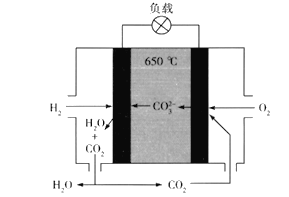
A. 电池工作时,熔融碳酸盐只起到导电的作用
B. 负极反应式为H2 -2e- +CO32-==CO2+H2O
C. 该电池可利用工厂中排出的CO2,减少温室气体的排放
D. 电池工作时,外电路中流过0.2 mol电子,消耗3.2 g O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t ℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_________________________________。
(2)该反应为________反应(填“吸热”或“放热”)。
(3)某温度下,各物质的平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为______。
(4)若830 ℃时,向容器中充入1 mol CO、5 mol H2O,反应达到平衡后,其化学平衡常数K______1.0(填“大于”“小于”或“等于”)。
(5)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的体积。平衡____移动(填“向正反应方向”“向逆反应方向”或“不”)。
(6)若1 200 ℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时上述反应的平衡移动方向为__________(填“正反应方向”“逆反应方向”或“不移动”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com