
| A£® | 1 mol CH3COOKµÄÖŹĮæĪŖ98 g•mol-1 | |
| B£® | CH3COOKµÄĦ¶ūÖŹĮæµČÓŚĖüµÄĻą¶Ō·Ö×ÓÖŹĮæ | |
| C£® | Ņ»øöCH3COOKĪ¢Į£µÄÖŹĮæŌ¼ĪŖ98 g/NA | |
| D£® | ŗ¬ÓŠ6.02”Į1023øöĢ¼Ō×ÓµÄCH3COOKµÄĪļÖŹµÄĮæĪŖ1 mol |
·ÖĪö A£®ÖŹĮæµÄµ„Ī»ŹĒg£»
B£®ŹżÖµÉĻ£¬ĪļÖŹµÄĦ¶ūÖŹĮæµČÓŚĘäĻą¶Ō·Ö×ÓÖŹĮ棻
C£®Ņ»øöCH3COOKĪ¢Į£µÄÖŹĮæ=$\frac{M}{{N}_{A}}$g£»
D£®Ņ»øö“×Ėį¼Ų»ÆѧŹ½ÖŠŗ¬ÓŠĮ½øöĢ¼Ō×Ó£¬“×Ėį¼ŲµÄĪļÖŹµÄĮæŹĒĢ¼Ō×ÓĪļÖŹµÄĮæµÄŅ»°ė£®
½ā“š ½ā£ŗA.1molCH3COOKµÄÖŹĮæĪŖ98 g£¬¹ŹA“ķĪó£»
B£®Ä¦¶ūÖŹĮæµÄµ„Ī»ŹĒg/mol£¬Ļą¶Ō·Ö×ÓÖŹĮæµÄµ„Ī»ŹĒ”°1”±£¬¹ŹB“ķĪó£»
C£®Ņ»øöCH3COOKĪ¢Į£µÄÖŹĮæ=$\frac{M}{{N}_{A}}$g=$\frac{98}{6.02”Į1{0}^{23}}$g£¬¹ŹCÕżČ·£»
D£®“×Ėį¼ŲµÄĪļÖŹµÄĮæŹĒĢ¼Ō×ÓĪļÖŹµÄĮæµÄŅ»°ė£¬ĪŖ0.5mol£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖÓŠ¹ŲĦ¶ūÖŹĮæµÄÖŖŹ¶£¬ÄŃ¶Č²»“ó£¬×¢ŅāĻą¶Ō·Ö×ÓÖŹĮæÓŠµ„Ī»£¬ĒŅµ„Ī»ŹĒ”°1”±£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4+µÄµē×ÓŹżĪŖ10 | B£® | H218OµÄ·Ö×ÓĮæĪŖ18 | ||
| C£® | BeµÄ×īĶā²ćÓŠ1øöµē×Ó | D£® | H-µÄµē×Ó²ćŹżÓŠ2²ć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 HS-+H+
HS-+H+²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČĘųŹĒŅ»ÖÖĪŽÉ«”¢ĆܶȱČæÕĘų“óµÄÓŠ¶¾ĘųĢå | |
| B£® | ŗģČȵÄĢśĖæŌŚCl2ÖŠ¾ēĮŅČ¼ÉÕÉś³ÉFeCl2 | |
| C£® | ŠĀÖĘĀČĖ®ÄÜɱ¾śĻū¶¾ŹĒŅņĪŖCl2ÓŠ¶¾£¬Äܶ¾É±Ļø¾ś | |
| D£® | ĀČĖ®·ÅÖĆŹżĢģŗóĖįŠŌŌöĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
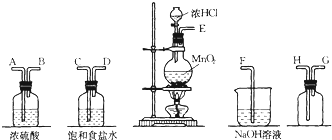
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | R±ķŹ¾·Ē“¦·½Ņ©£¬OTC±ķŹ¾“¦·½Ņ© | |
| B£® | Ź¹ÓĆĒąĆ¹ĖŲŹ±£¬Ö±½Ó¾²Āö×¢ÉäæÉŅŌ²»ÓĆ½ųŠŠĘ¤·ōĆōøŠŹŌŃé | |
| C£® | ³¤ĘŚ“óĮæŹ¹ÓĆ°¢Ė¾Ę„ĮÖæÉŅŌŌ¤·ĄÄ³Š©¼²²”£¬Ć»ÓŠČĪŗĪø±×÷ÓĆ | |
| D£® | °¢Ė¾Ę„ĮÖŹōÓŚ½āČČÕņĶ“Ņ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉżøßĪĀ¶ČÄܼÓæģ·“Ó¦ĖŁĀŹ | |
| B£® | Ź¹ÓĆĒ”µ±µÄ“߻ƼĮÄܼÓæģ·“Ó¦ĖŁĀŹ | |
| C£® | Ōö“óN2µÄÅضČÄܼÓæģ·“Ó¦ĖŁĀŹ | |
| D£® | Ņ»¶ØĢõ¼žĻĀ“ļµ½Ę½ŗāŹ±£¬N2ÓėH2µÄÅØ¶Č±ČŅ»¶ØŹĒ1©s3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉŁĮæÅØĮņĖįÕ“ŌŚĘ¤·ōÉĻ£¬Į¢¼“ÓĆĒāŃõ»ÆÄĘČÜŅŗ³åĻ“ | |
| B£® | ÕōĮó²Ł×÷Ź±£¬Ó¦Ź¹ĪĀ¶Č¼ĘĖ®ŅųĒņææ½üÕōĮóÉÕĘæÖ§¹ÜæŚ“¦ | |
| C£® | ŹµŃéŹŅæÉÓĆČ¼×ÅµÄ¾Ę¾«µĘČ„µćČ¼ĮķŅ»Ö»¾Ę¾«µĘ | |
| D£® | ½«ŗ¬ĮņĖįµÄ·ĻŅŗµ¹ČėĖ®²Ū£¬ÓĆĖ®³åČėĻĀĖ®µĄ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com