
【题目】某同学设计了如下实验装置,进行浓硫酸与蔗糖的反应实验。

(1)实验开始时,先在烧瓶中加入15g蔗糖,并滴入几滴水使蔗糖完全湿润,然后从分液漏斗中加入15mL浓硫酸,水的作用是_________。
(2)实验中烧瓶内黑色物质疏松膨胀的原因是________(用化学方程式表示)。
(3)为了检验实验中产生的CO2,请描述接口a之后的实验操作及现象_________
【答案】与浓硫酸反应放热,加快反应速率 C+2H2SO4(浓)![]() 2SO2↑+CO2↑+2H2O 将接口a处的气体,依次通过高锰酸钾溶液、品红溶液、澄清石灰水,如果品红溶液不褪色,石灰水变浑浊,说明实验中产生了CO2气体
2SO2↑+CO2↑+2H2O 将接口a处的气体,依次通过高锰酸钾溶液、品红溶液、澄清石灰水,如果品红溶液不褪色,石灰水变浑浊,说明实验中产生了CO2气体
【解析】
本题考查的是浓硫酸的性质。
(1)浓硫酸有三大特性:吸水性、脱水性、强氧化性。先在烧瓶中加入15g蔗糖,并滴入几滴水使蔗糖完全湿润,然后从分液漏斗中加入15mL浓硫酸,浓硫酸滴到蔗糖上使蔗糖脱水,滴入水的作用是与浓硫酸反应放热,加快反应速率。
(2)浓硫酸滴到蔗糖上使蔗糖脱水碳化,碳与浓硫酸反应生成二氧化碳、二氧化硫和水。由于有气体生成使烧瓶内黑色物质疏松膨胀。
(3)由于SO2与CO2的性质相似,均能使澄清的石灰水变浑浊,SO2干扰CO2的检验,则为检验实验中产生的CO2,接口a处的气体,应先通过高锰酸钾溶液除去SO2,在通过品红溶液检验SO2是否除尽,再通过澄清石灰水检验CO2。如果品红溶液不褪色,石灰水变浑浊,说明实验中产生了CO2气体。
(1)浓硫酸有三大特性:吸水性、脱水性、强氧化性。先在烧瓶中加入15g蔗糖,并滴入几滴水使蔗糖完全湿润,然后从分液漏斗中加入15mL浓硫酸,浓硫酸滴到蔗糖上使蔗糖脱水,滴入水的作用是与浓硫酸反应放热,加快反应速率。本小题答案为:与浓硫酸反应放热,加快反应速率。
(2)浓硫酸滴到蔗糖上使蔗糖脱水碳化,碳与浓硫酸反应生成二氧化碳、二氧化硫和水。由于有气体生成使烧瓶内黑色物质疏松膨胀。本小题答案为:C+2H2SO4(浓)![]() 2SO2↑+CO2↑+2H2O。
2SO2↑+CO2↑+2H2O。
(3)由于SO2与CO2的性质相似,均能使澄清的石灰水变浑浊,SO2干扰CO2的检验,则为检验实验中产生的CO2,接口a处的气体,应先通过高锰酸钾溶液除去SO2,在通过品红溶液检验SO2是否除尽,再通过澄清石灰水检验CO2。如果品红溶液不褪色,石灰水变浑浊,说明实验中产生了CO2气体。本小题答案为:将接口a处的气体,依次通过高锰酸钾溶液、品红溶液、澄清石灰水,如果品红溶液不褪色,石灰水变浑浊,说明实验中产生了CO2气体。


科目:高中化学 来源: 题型:
【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)装置A是氯气的发生装置,请写出相应反应的化学方程式:__________。
(2)装置B中饱和食盐水的作用是___________;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:_______________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III处依次放入物质的组合应是_________填字母编号)。
编号 | I | II | III |
a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是__________________________,该现象__________(填“能”或“不能”)说明溴单质的氧化性强于碘,原因是____________。
(5)装置F的作用是__________________,其烧杯中的溶液不能选用下列中的_____(填字母编号)。
a.饱和NaOH溶液 b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液 d.饱和Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如图。
下列有关叙述不正确的是
A. H +从负极区通过交换膜移向正极区
B. 电池总反应为2CH3OH+3O2===2CO2+4H2O
C. 负极的电极反应式为:CH3OH+ H2O-6e-=CO2↑+ 6H +
D. 图中b、c分别是O2、甲醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究人员将Cu与Cu2O的混合物ag,用足量的稀H2SO4充分反应后,剩余固体质量为bg。
已知:Cu2O+2H+═Cu+Cu2++H2O
(1)混合物中n(Cu2O)=________mol(用含a、b的最简式表示)
(2)若将ag混合物在空气中加热生成CuO,则m(CuO)=_______g(用含a、b的最简式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氧化还原反应中,水作为氧化剂的是( )
A. CO+H2O![]() CO2+H2B. CuO+H2
CO2+H2B. CuO+H2![]() Cu+H2O
Cu+H2O
C. 2F2+2H2O═4HF+O2D. 3NO2+H2O═2HNO3+NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1 ;
2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) ΔH2,
则ΔH1______ΔH2;(填“> ”、“< ”或“=”)
(2)已知:H2(g)+Cl2(g)===2HCl(g)ΔH=-185 kJ·mol-1,查阅资料可知:H—H键能:436 kJ·mol-1、Cl—Cl键能:243 kJ·mol-1,则H—Cl键能=______________;
(3)在298K、100kPa时,已知:2H2(g)+O2(g)==2H2O(g) ΔH1 ;2HCl(g)==Cl2(g)+H2(g) ΔH2 ;2Cl2(g)+2H2O(g)==4HCl(g)+O2(g)ΔH3 , 则ΔH3与ΔH1和ΔH2的关系是:ΔH3=_______________;
(4)消除氮氧化物的污染对环境至关重要,用CH4催化还原NOx可以消除氮氧化物的污染。已知一定条件下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1
则该条件下,用CH4还原NO2至N2的热化学方程式为:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了如下实验装置,进行浓硫酸与蔗糖的反应实验。

(1)实验开始时,先在烧瓶中加入15g蔗糖,并滴入几滴水使蔗糖完全湿润,然后从分液漏斗中加入15mL浓硫酸,水的作用是_________。
(2)实验中烧瓶内黑色物质疏松膨胀的原因是________(用化学方程式表示)。
(3)为了检验实验中产生的CO2,请描述接口a之后的实验操作及现象_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析图,甲、乙具有的共性是
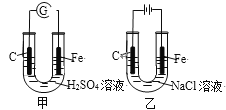
A. 反应物能量均高于生成物能量
B. 电极反应均有Fe-2e→Fe2+
C. 碳棒上均发生氧化反应
D. 溶液pH均增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com