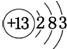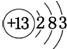某同学欲制取相同体积(同温同压)的氢气,他称取了两份铝粉,第一份加足量NaOH溶液,第二份加足量盐酸,则
(1)铝在元素周期表中的位置为 其原子结构示意图为
(2)涉及反应的离子方程式分别为 ,
(3)如果要得到相同体积(同温同压)的氢气,两份铝粉的质量比为 .
【答案】
分析:(1)根据原子序数写出原子结构示意图,再根据电子层数等周期序数,最外层电子数等于主族序数,判断元素周期表中的位置;
(2)根据反应写出离子方程式
(3)根据铝跟盐酸或氢氧化钠溶液都能发生反应生成氢气的化学方程式即可看出生成氢气的多少.
解答:解:(1)因铝的原子序数为13,所以其原子结构示意图为

,所以在元素周期表中的位置为第三周期、第IIIA族;
(2)因铝粉与盐酸或氢氧化钠溶液反应,其化学方程式分别为:2Al+6HCl=2AlCl
3+3H
2↑;2Al+2NaOH+2H
2O=2NaAlO
2+3H
2↑
(3)因铝粉与盐酸或氢氧化钠溶液反应都能放出氢气:2Al+6HCl=2AlCl
3+3H
2↑,2Al+2NaOH+2H
2O=2NaAlO
2+3H
2↑,
由反应的化学方程式可以得知,相同条件下,等质量的铝分别跟足量的稀盐酸、NaOH溶液反应,放出氢气的质量都是3H
2,因此,放出氢气的质量一样多.
故答案为:(1)第三周期 第IIIA族;

;
(2)2Al+6H
+=Al
3++3H
2↑;2Al+2OH
-+2H
2O=2AlO
2-+3H
2↑;
(3)1:1
点评:本题主要考查学生对参加反应的物质质量的计算能力.学生需正确书写出化学方程式,然后根据化学方程式找出比例关系,列出比例式,并正确分析各物质之间的关系,才能正确答题.

 ,所以在元素周期表中的位置为第三周期、第IIIA族;
,所以在元素周期表中的位置为第三周期、第IIIA族; ;
;