
【题目】写出下对反应的化学方程式,并注明反应类型:
(1)乙醇制乙烯:_________________,反应类型:_________________。
(2)乙醇与浓氢溴酸反应:_________________,反应类型_________________。
(3)苯酚与浓溴水反应:_________________,反应类型_________________。
(4)乙醛与银氨溶液反应:_________________,反应类型_________________。
(5)乙醛与新制氢氧化铜悬浊液反应:_________________,反应类型_________________。
(6)乙酸乙酯与氢氧化钠溶液反应:_________________,反应类型_________________。
【答案】CH3—CH2OH![]() CH2=CH2↑+H2O 消去反应 CH3CH2OH+HBr
CH2=CH2↑+H2O 消去反应 CH3CH2OH+HBr![]() CH3—CH2—Br+H2O 取代反应
CH3—CH2—Br+H2O 取代反应 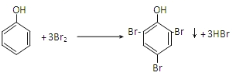 取代反应 CH3—CHO+2Ag(NH3)2OH
取代反应 CH3—CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag↓+3NH3+H2O 氧化反应 CH3CHO+2Cu(OH)2
CH3COONH4+2Ag↓+3NH3+H2O 氧化反应 CH3CHO+2Cu(OH)2![]() CH3COOH+Cu2O↓+2H2O 氧化反应 CH3COOC2H5+NaOH→CH3COONa+CH2OH 取代反应
CH3COOH+Cu2O↓+2H2O 氧化反应 CH3COOC2H5+NaOH→CH3COONa+CH2OH 取代反应
【解析】
(1)乙醇与浓硫酸混合加热到170℃发生消去反应生成乙烯,反应的化学方程式为:CH3CH2OH![]() CH2=CH2↑+H2O,属于消去反应;
CH2=CH2↑+H2O,属于消去反应;
故答案为:CH3CH2OH![]() CH2=CH2↑+H2O;消去反应。
CH2=CH2↑+H2O;消去反应。
(2)乙醇与浓氢溴酸发生取代反应生成溴乙烷和水,反应的化学方程式为CH3CH2OH+HBr![]() CH3CH2Br+H2O,属于取代反应;
CH3CH2Br+H2O,属于取代反应;
故答案为:CH3CH2OH+HBr![]() CH3CH2Br+H2O,取代反应。
CH3CH2Br+H2O,取代反应。
(3)苯酚与浓溴水反应,是苯酚分子中羟基对苯环影响,邻对位氢原子活泼,反应的化学方程式为:  ,属于取代反应,
,属于取代反应,
故答案为: 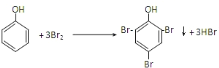 ,取代反应。
,取代反应。
(4)乙醛发生银镜反应,是醛基的还原性,被弱氧化剂氧化为乙酸,反应的化学方程式为:CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag↓+3NH3+H2O,属于氧化反应,
CH3COONH4+2Ag↓+3NH3+H2O,属于氧化反应,
故答案为:CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag↓+3NH3+H2O,氧化反应。
CH3COONH4+2Ag↓+3NH3+H2O,氧化反应。
(5)乙醛与新制氢氧化铜悬浊液反应,是醛基的还原性,被弱氧化剂氧化为乙酸,反应的化学方程式为:CH3CHO+2Cu(OH)2![]() CH3COOH+Cu2O↓+2H2O,属于氧化反应,
CH3COOH+Cu2O↓+2H2O,属于氧化反应,
故答案为:CH3CHO+2Cu(OH)2![]() CH3COOH+Cu2O↓+2H2O,氧化反应。
CH3COOH+Cu2O↓+2H2O,氧化反应。
(6)乙酸乙酯在碱性条件下完全水解生成乙酸钠、乙醇,反应的化学方程式为:CH3COOC2H5+NaOH→CH3COONa+CH2OH,属于取代反应;
故答案为:CH3COOC2H5+NaOH→CH3COONa+CH2OH,取代反应。


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】有五种短周期元素,它们的结构、性质等信息如下表所述:
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | B与A同周期,其最高价氧化物的水化物呈两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
E | L层上有2对成对电子 |
请根据表中信息填空:
(1)A原子的核外电子排布式为___________。
(2)B元素在周期表中的位置:__________________;离子半径:B___ A(填“大于”或“小于”)
(3)C原子的价电子排布图是___________,其原子核外有__________个未成对电子,能量最高的电子为___________轨道上的电子,其轨道呈___________形。
(4)D原子的电子排布式为___________。D-的结构示意图是________________
(5)C、E元素的第一电离能的大小关系是___________(用元素符号表示)。
(6)已知CD3分子中D元素为+1价,则C、D的电负性大小关系是________________(用元素符号表示),CD3与水反应后的产物是__________和__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示转化关系(部分产物已略去)。下列说法正确的是( )
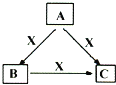
A. 若X为KOH溶液,则A可能为Al
B. 若X为Fe,则C可能为Fe(NO3)2溶液
C. 若A、B、C均为焰色反应呈黄色的化合物,则X一定为CO2
D. 若X为O2,则A可为有机物乙醇,也可为非金属单质硫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如下图所示,下列叙述错误的是
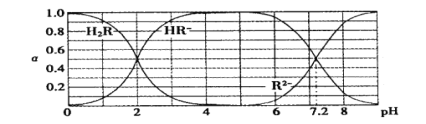
A.H2R是二元弱酸,其Ka1=1×10-2
B.当溶液恰好呈中性时,c( Na + )=2c ( R2- ) + c( HR- )
C.NaHR在溶液中水解倾向大于电离倾向
D.含Na2R与NaHR各0.1 mol的混合溶液的pH=7.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两个完全相同的装置,分别在它们的侧管中装入1.06g Na2CO3和0.84g NaHCO3,试管中各有10mL相同浓度的盐酸(如图),同时将两个侧管中的物质全部倒入各自的试管中,下列叙述正确的是
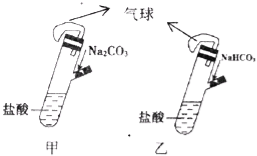
A. 甲装置的气球膨胀速率大
B. 若最终两气球体积相同,则一定有c(HCl)≥2 mol/L
C. 若最终两气球体积不同,则一定有c(HCl)≤1 mol/L
D. 最终两溶液中Na+、Cl﹣的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
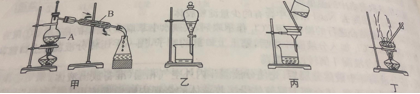
(1)为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
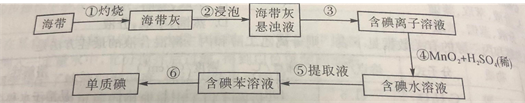
a.灼烧海带时,除需要三脚架外,还需要用到实验仪器是_____(填字母)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
b.步骤③的实验选择上述图_____(填“甲”“乙”或“丙”)装置。步骤⑤的实验操作名称是_____,选择上述图_____(填“甲”“乙”或“丙”)装置。步骤⑥的目的是从含碘苯溶液中分离出单子碘,同时回收苯,该步骤的实验操作名称是_____,选择上述图_____(填“甲”“乙”或“丙”)装置。
(2)某盐的混合溶液中含有Na+、Mg2+、Cl-、SO42-离子,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为0.2molL-1、0.25molL-1、0.4molL-1,则c(SO42-)=_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以溴乙烷为原料制备乙二醇,下列方案中最合理的是
A. CH3CH2Br![]() CH2=CH2
CH2=CH2![]() CH2BrCH2Br
CH2BrCH2Br![]() 乙二醇
乙二醇
B. CH3CH2Br![]() CH2BrCH2Br
CH2BrCH2Br![]() 乙二醇
乙二醇
C. CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH2BrCH2OH
CH2BrCH2OH![]() 乙二醇
乙二醇
D. CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH2=CH2
CH2=CH2![]() CH2BrCH2Br
CH2BrCH2Br![]() 乙二醇
乙二醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取乙炔并验证其性质的装置图。下列说法不合理的是

A. 将生成的气体直接通入到溴水中,溴水褪色,说明有乙炔生成
B. 酸性KMnO4溶液褪色,说明乙炔具有还原性
C. 逐滴加入饱和食盐水可控制生成乙炔的速率
D. 将纯净的乙炔点燃,有浓烈的黑烟,说明乙炔不饱和程度高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1 mol·L1稀盐酸,CO2的生成量与加入盐酸的体积的关系如图。下列判断正确的是
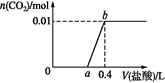
A. 在0~a范围内,只发生中和反应
B. ab段发生反应的离子方程式为:![]()
C. a=0.3
D. 原混合溶液中NaOH与Na2CO3的物质的量之比为1∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com