
| A. | 磁性氧化铁溶于稀硝酸:Fe3O4+8H++NO3-═3Fe3++NO↑+4H2O | |
| B. | Ca(HCO3)2溶液中加入过量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| C. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O |
分析 A.硝酸具有氧化性,反应生成铁离子和水;
B.氢氧化钠过量,反应生成碳酸钙、碳酸钠和水;
C.氢氧化钠过量,铵根离子、碳酸氢根离子都反应;
D.离子个数配比不符合物质结构组成.
解答 解:A.将磁性氧化铁溶于足量稀硝酸中的离子反应为3Fe3O4+NO3-+28H+═9Fe3++14H2O+NO↑,故A错误;
B.Ca(HCO3)2溶液中加入过量NaOH溶液,离子方程式:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O,故B正确;
C.NH4HCO3溶于过量的NaOH溶液中,离子方程式:NH4++HCO3-+2OH-═CO32-+H2O+NH3•H2O,故C错误;
D.氢氧化钡溶液与稀硫酸反应,离子方程式:Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O,故D错误;
故选:B.
点评 本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意氧化还原反应中电子守恒,题目难度不大.


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源:2016-2017学年江苏省徐州市高一上第一次月考化学卷(解析版) 题型:选择题
下列反应属于加成反应的是
A.CH4+Cl2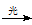 CH3Cl+HCl
CH3Cl+HCl
B.CH2===CH2+HBr→CH3CH2Br
C.CH3COOH+CH3CH2OH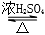 CH3COOCH2CH33+H2O
CH3COOCH2CH33+H2O
D.2CH3CH2OH+O2 2CH3CHO+2H2O
2CH3CHO+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铈(Ce)元素在自然界中主要以化合态形式存在 | |
| B. | 铈溶于氢碘酸的化学方程式可表示为:Ce+4HI═CeI4+2H2↑ | |
| C. | 用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+═Ce3++Fe3+ | |
| D. | 四种稳定的核素58136Ce、58138Ce、58140Ce、58142Ce,它们互称为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-浓度为0.2 mol/L | |
| B. | 取出10 mL溶液中Ba2+浓度为0.2 mol/L | |
| C. | 溶液中Cl-总数为0.2NA | |
| D. | 取出50 mL溶液中Ba2+和Cl-总数为0.03NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol CO+2.0 mol H2O(g)+1.0 mol CO2+1.0 mol H2 | |
| B. | 1.0 mol CO+2.0 mol H2O(g)+0.5 mol He | |
| C. | 1.0 mol CO+1.0 mol H2O(g)+1.0 mol CO2+1.0 mol H2 | |
| D. | 0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 轮船水线以下的船壳上装上一定数量的锌块 | |
| B. | 银质奖章久置后表面变暗 | |
| C. | 黄铜(铜锌合金)制作的铜锣不易产生铜绿 | |
| D. | 纯锌与稀H2SO4反应滴入少量的CuSO4溶液后反应速率加快 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第一次月考化学试卷(解析版) 题型:选择题
下列是4位同学在学习“化学反应速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是( )
A. 化学反应速率理论是研究怎样在一定时间内快出产品
B. 化学平衡理论是研究怎样使用有限原料多出产品
C. 化学平衡理论是研究怎样使原料尽可能多地转化为产品
D. 化学反应速率理论是研究怎样提高原料转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com