
钢铁“发蓝”是将钢铁制品浸到某些氧化性的溶液中,在钢铁的表面形成一层四氧化三铁的技术过程。其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热到130 ℃反应。其过程可以用如下化学方程式表示:
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
②6Na2FeO2+NaNO2+=5H2O3Na2Fe2O4+NH3↑+7NaOH
③Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH下列说法正确的是( )。
A.反应①不是氧化还原反应
B.该生产过程不产生任何污染
C.整个反应过程中,每有5.6 g Fe参加反应转移0.8 mol电子
D.反应②中的氧化剂是NaNO2
科目:高中化学 来源:2014年高二化学苏教版选修2 5专题综合检测练习卷(解析版) 题型:填空题
丙烯可用于合成杀除根瘤线虫的农药(分子式为C3H5Br2Cl)和应用广泛的DAP树脂:
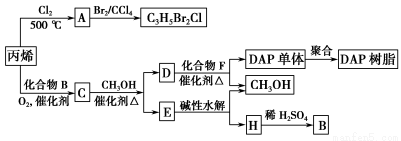
已知酯与醇可发生如下酯交换反应:
RCOOR′+R″OHRCOOR″+R′OH(R、R′,R″代表烃基)
(1)农药C3H5Br2Cl分子中每个碳原子上均连有卤原子。
①A的结构简式是____________________________________________________,
A含有的官能团名称是________;
②由丙烯生成A的反应类型是________。
(2)A水解可得到D,该水解反应的化学方程式是_____________________________________。
(3)C蒸气密度是相同状态下甲烷密度的6.25倍,C中各元素的质量分数分别为:碳60%,氢8%,氧32%。C的结构简式是________。
(4)下列说法正确的是(选填序号字母)________。
a.C能发生聚合反应、还原反应和氧化反应
b.C含有2个甲基的羧酸类同分异构体有4个
c.D催化加氢的产物与B具有相同的相对分子质量
d.E具有芳香气味,易溶于乙醇
(5)E的水解产物经分离最终得到甲醇和B,二者均可循环用于DAP树脂的制备。其中将甲醇与H分离的操作方法是________。
(6)F的分子式为C10H10O4。DAP单体为苯的二元取代物,且两个取代基不处于对位,该单体苯环上的一溴取代物只有两种。D和F反应生成DAP单体的化学方程式是_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 4专题综合检测练习卷(解析版) 题型:填空题
晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl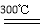 SiHCl3+H2;
SiHCl3+H2;
③SiHCl3与过量H2在1 000~1 100 ℃反应制得纯硅已知SiHCl3能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第①步制备粗硅的化学方程式为_____________________________________________。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0 ℃)中含有少量SiCl4(沸点57.6 ℃)和HCl(沸点-84.7 ℃),提纯SiHCl3采用的方法为___________________________。
(3)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):
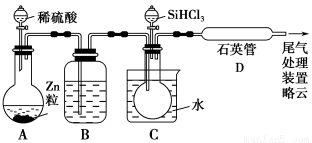
①装置B中的试剂是________。装置C中的烧瓶需要加热,其目的是________________________________________________________________。
②反应一段时间后,装置D中观察到的现象是________,装置D不能采用普通玻璃管的原因是____________,装置D中发生反应的化学方程式为_____________________________________________________________。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 4.3复合材料的制造练习卷(解析版) 题型:选择题
我国及美国、日本等国家都已研制出一种陶瓷柴油机,这种柴油机的发动机部件的受热面是用一种耐高温且不易传热的材料来制造的,这种材料是( )。
A.氧化铝陶瓷 B.氮化硅陶瓷
C.光导纤维 D.玻璃钢
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 4.2材料组成的优化练习卷(解析版) 题型:选择题
光纤通信是一种现代化的通信手段,它可以提供大容量、高速度、高质量的通信服务。目前,我国正在大力建设高质量的宽带光纤通信网络,即信息高速公路。光纤通信所使用的光缆,其主要部件为光导纤维。下列说法正确的是( )。
①制造光导纤维的主要原料是CaCO3;②制造光导纤维的主要原料是SiO2;③光导纤维传递光信号的基本物理原理是光的全反射;④光导纤维传递光信号的基本物理原理是光的折射
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题3氧化还原反应练习卷(解析版) 题型:填空题
已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是________,被氧化的离子的物质的量分别是________________。
(2)如果向原溶液中通入3 mol Cl2,则被氧化的离子是________,其对应氧化产物的物质的量分别是________________。
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:S2O82—+2I-=2SO42—+I2。通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应的催化过程:______________________________、____________________________(不必配平)。
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题3氧化还原反应练习卷(解析版) 题型:选择题
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,蓝色溶液变为棕色。再向反应后的溶液中通入过量的SO2气体,溶液变成无色。则下列说法正确的是( )
A.滴加KI溶液时,KI被氧化,CuI是氧化产物
B.通入SO2后溶液逐渐变成无色,体现了SO2的漂白性
C.通入22.4 L SO2参加反应时,有2NA个电子发生转移
D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题2化学常用计量练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列说法不正确的是( )
A.常温下,1 L pH=1的硫酸溶液中含有的H+为0.1NA
B.常温下,14 g C2H4和C3H6的混合气体中含有2NA个氢原子
C.2.3 g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1NA
D.1 mol甲醇中含有C—H键的数目为NA
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 3.1有机药物制备练习卷(解析版) 题型:选择题
在阿司匹林的结构简式中①②③④⑤⑥分别标出了其分子中的不同的键。将阿司匹林与足量NaOH溶液共煮时,发生反应时断键的位置是( )。
A.①④ B.②⑤ C.③④ D.②⑥

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com