
| 选项 | 实验操作 | 现象 | 结论 |
| A | 测定常温时的饱和HCOONa溶液、CH3COONa溶液的pH | HCOONa的pH<CH3COONa的pH | 弱酸的酸性:HCOOH>CH3COOH |
| B | 向5ml2mol•L-1 NaOH溶液中加入1ml 1mol•L-1 CuSO4溶液,振荡后加入0.5ml有机物X,加热 | 未出现砖红色沉淀 | 说明X中不含有醛基 |
| C | KBrO3溶液中加入少量苯,然后通入少量Cl2 | 有机相呈橙红色 | 氧化性:Cl2>Br2 |
| D | NaAlO2溶液与NaHCO3溶液混合 | 有白色絮状沉淀生成 | 二者水解相互促进生成氧化铝沉淀 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二者溶解度不同,饱和时浓度不同,无法比较水解程度大小;
B.含有醛基的有机物能够与新制氢氧化铜反应生成砖红色的氧化亚铜沉淀;
C.有机相呈橙色,说明该反应中有Br2生成,Br元素化合价由+5价变为0价,所以KBrO3是氧化剂,则Cl2是还原剂;
D.碳酸氢根离子的酸性大于氢氧化铝,二者发生的是强酸制取弱酸的反应,不是双水解反应.
解答 解:A.饱和HCOONa溶液和CH3COONa溶液的浓度不相同,无法比较二者的水解程度,则无法比较HCOOH、CH3COOH的酸性强弱,故A错误;
B.向5ml 2mol•L-1 NaOH溶液中加入1ml 1mol•L-1 CuSO4溶液可以制备氢氧化铜浊液,振荡后加入0.5ml有机物X,加热,该操作方法合理,若未出现砖红色沉淀,说明说明X中不含有醛基,故B正确;
C.KBrO3溶液中加入少量苯,然后通入少量Cl2,有机相呈橙色,说明该反应中有Br2生成,Br元素化合价由+5价变为0价,所以KBrO3是氧化剂,则Cl2是还原剂,说明氧化性:Cl2<KBrO3,无法得出氧化性Cl2>Br2,故C错误;
D.由于碳酸氢根离子的酸性大于氢氧化铝,NaAlO2溶液与NaHCO3溶液混合后生成氢氧化铝沉淀和碳酸钠,没有发生双水解反应,故D错误;
故选B.
点评 本题考查化学实验方案的评价,题目难度不大,涉及氧化还原反应、盐的水解原理、醛基检验等知识,明确常见元素及其化合物性质即可解答,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 复分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “时气错逆,霾雾蔽日”,雾所形成的气溶胶能产生丁达尔效应 | |
| B. | “青蒿一揭,以水二升溃,绞取汁”,屠呦呦提取青蒿素的过程中发生了化学变化 | |
| C. | “熬胆矾铁釜,久之亦化为铜”,北宋沈括用胆矾炼铜的过程属于置换反应 | |
| D. | “外观如雪,强烧之,紫青烟起”,南北朝陶弘景对硝酸钾的鉴定过程中利用了焰色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10mL18mol/L浓硫酸与足量铜加热充分反应,转移电子数为0.18NA | |
| B. | 11gT2O超重水中含有的中子数为5NA | |
| C. | 标准状况下,22.4LCO2中含有的共用电子对数为2NA | |
| D. | 7.8 gNa2S固体和7.8gNa2O2固体中含有的阴离子数目均为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下是一种无色无味的液体 | B. | 能与乙醇发生酯化反应 | ||
| C. | 不能与NaHCO3反应放出CO2 | D. | 能与溴水发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
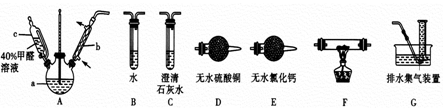

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 所示的是战国初期的曾侯乙编钟,它是一套庞大的青铜乐器.铸造该器物的主要材料是b(填字母,下同).
所示的是战国初期的曾侯乙编钟,它是一套庞大的青铜乐器.铸造该器物的主要材料是b(填字母,下同).
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法正确的是( )
25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法正确的是( )| A. | 点①所示溶液中:c(H+)+c(H2C2O4)+c(HC2O4-)=c(OH-) | |
| B. | 点②所示溶液中:c(H2C2O4)+c(HC2O4-)+c(C2O42-)=c(Na+) | |
| C. | 点③所示溶液中:c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) | |
| D. | 滴定过程中可能出现:c(Na+)>c(C2O42-)=c(HC2O4-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 两个容积均为2L 的密闭容器I和Ⅱ中发生反应2NO(g)+2CO(g)?N2(g)+2CO(g),起始物质的量见表.
两个容积均为2L 的密闭容器I和Ⅱ中发生反应2NO(g)+2CO(g)?N2(g)+2CO(g),起始物质的量见表.| 容器 | 起始物质的量 | |
| NO | CO | |
| Ⅰ | 1mol | 3mol |
| Ⅱ | 6mol | 2mol |
| A. | N点的平衡常数为0.04L/mol | |
| B. | M、N两点容器内的压强:P(M)>2P(N) | |
| C. | 若将容器I的容积改为1L,T1温度下达到平衡时c(CO2)=0.25mol/L | |
| D. | 若将容器Ⅱ改为绝热容器,实验起始温度为T1,达平衡时NO的转化率大于16.7% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com