
”¾ĢāÄæ”æŹŅĪĀ£¬ĻĀĮŠĖÄÖÖČÜŅŗÖŠ£¬ÓÉĖ®µēĄėÉś³ÉµÄĒāĄė×ÓÅضČÖ®±Č¢Ł”Ć¢Ś”Ć¢Ū”Ć¢ÜŹĒ(””””)
¢ŁpH=0µÄŃĪĖį¢Ś0.1 mol/LµÄĒāµāĖį¢Ū0.01 mol/LµÄNaOHČÜŅŗ
¢ÜpH=11µÄ°±Ė®
A. 1”Ć10”Ć100”Ć1 000 B. 0”Ć1”Ć12”Ć11
C. 14”Ć13”Ć12”Ć11 D. 14”Ć13”Ć2”Ć3
”¾“š°ø”æA
”¾½āĪö”æŌŚĖįČÜŅŗÖŠ£¬OH£ŹĒĖ®µēĄė²śÉśµÄ£¬ŌŚ¼īČÜŅŗÖŠ£¬H+ŹĒĖ®µēĄė²śÉśµÄ£¬ĒŅĖ®µēĄė²śÉśµÄĒāĄė×ÓÅØ¶ČµČÓŚĖ®µēĄė²śÉśµÄĒāŃõøłĄė×ÓÅØ¶Č”£¢ŁpH=0µÄŃĪĖį£¬ČÜŅŗÖŠĒāĄė×ÓÅضČĪŖ1mol/L£¬Ė®µēĄė²śÉśµÄĒāŃõøłĄė×ÓÅضČĪŖ£ŗ ![]() mol/L=1”Į10£14mol/L£¬ŌņĖ®µēĄė²śÉśµÄĒāĄė×ÓÅضČĪŖ1”Į10£14mol/L£»¢Ś0.1 mol/LµÄĒāµāĖį£¬ĒāµāĖįŹĒŅ»ŌŖĒæĖį£¬ŌņČÜŅŗÖŠµÄĒāĄė×ÓÅضČĪŖ0.1mol/L£¬ÓÉĖ®µēĄė²śÉśµÄĒāŃõøłĄė×ÓÅضČĪŖ£ŗ
mol/L=1”Į10£14mol/L£¬ŌņĖ®µēĄė²śÉśµÄĒāĄė×ÓÅضČĪŖ1”Į10£14mol/L£»¢Ś0.1 mol/LµÄĒāµāĖį£¬ĒāµāĖįŹĒŅ»ŌŖĒæĖį£¬ŌņČÜŅŗÖŠµÄĒāĄė×ÓÅضČĪŖ0.1mol/L£¬ÓÉĖ®µēĄė²śÉśµÄĒāŃõøłĄė×ÓÅضČĪŖ£ŗ ![]() mol/L=1”Į10£13mol/L£¬ŌņĖ®µēĄė²śÉśµÄĒāĄė×ÓÅضČĪŖ1”Į10£13mol/L£»¢Ū0.01 mol/LµÄNaOHČÜŅŗÖŠ£¬ĒāŃõøłĄė×ÓÅضČĪŖ0.01 mol/L£¬ŌņÓÉĖ®µēĄė²śÉśµÄĒāĄė×ÓÅضČĪŖ£ŗ
mol/L=1”Į10£13mol/L£¬ŌņĖ®µēĄė²śÉśµÄĒāĄė×ÓÅضČĪŖ1”Į10£13mol/L£»¢Ū0.01 mol/LµÄNaOHČÜŅŗÖŠ£¬ĒāŃõøłĄė×ÓÅضČĪŖ0.01 mol/L£¬ŌņÓÉĖ®µēĄė²śÉśµÄĒāĄė×ÓÅضČĪŖ£ŗ ![]() mol/L=1”Į10£12mol/L£»¢ÜpH=11µÄ°±Ė®ČÜŅŗÖŠ£¬ĒāĄė×ÓÅضČĪŖ1”Į10£11mol/L£¬ŅņĒāĄė×ÓŹĒÓÉĖ®µēĄė²śÉśµÄ£¬ŌņÓÉĖ®µēĄė²śÉśµÄĒāĄė×ÓÅضČĪŖ1”Į10£11mol/L£¬Ņņ“ĖĖÄÖÖČÜŅŗÖŠ£¬ÓÉĖ®µēĄėÉś³ÉµÄĒāĄė×ÓÅضČÖ®±ČĪŖ£ŗ1”Į10£14: 1”Į10£13: 1”Į10£12: 1”Į10£11=1:10:100:1 000£¬¹Ź“š°øŃ”A”£
mol/L=1”Į10£12mol/L£»¢ÜpH=11µÄ°±Ė®ČÜŅŗÖŠ£¬ĒāĄė×ÓÅضČĪŖ1”Į10£11mol/L£¬ŅņĒāĄė×ÓŹĒÓÉĖ®µēĄė²śÉśµÄ£¬ŌņÓÉĖ®µēĄė²śÉśµÄĒāĄė×ÓÅضČĪŖ1”Į10£11mol/L£¬Ņņ“ĖĖÄÖÖČÜŅŗÖŠ£¬ÓÉĖ®µēĄėÉś³ÉµÄĒāĄė×ÓÅضČÖ®±ČĪŖ£ŗ1”Į10£14: 1”Į10£13: 1”Į10£12: 1”Į10£11=1:10:100:1 000£¬¹Ź“š°øŃ”A”£


 »īĮ¦æĪŹ±Ķ¬²½Į·Ļ°²įĻµĮŠ“š°ø
»īĮ¦æĪŹ±Ķ¬²½Į·Ļ°²įĻµĮŠ“š°ø ѧŅµ²āĘĄŅ»æĪŅ»²āĻµĮŠ“š°ø
ѧŅµ²āĘĄŅ»æĪŅ»²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµā»Æ±µ£ØBaI22H2O£©ŹĒŅ»ÖÖ°×É«·ŪÄ©£¬³£ÓĆÓŚÖĘČ”ĘäĖūŗ¬µā»ÆŗĻĪļ£®Ņ»ÖÖÖʱøĮ÷³ĢČēĶ¼1£ŗ 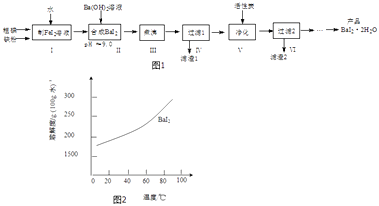
£Ø1£©²½Öč¢ńÖĘFeI2ČÜŅŗŹ±£¬Ģįøß·“Ó¦ĖŁĀŹµÄæÉŠŠ“ėŹ©ÓŠ£ØĢīŠņŗÅ£©£®
a£®Ģś·ŪŗĶµā·ŪÓĆĒņÄ„»śÄ„³ÉĻø·Ū
b£®Ōö“ón£ØĢś·Ū£©£ŗn£Øµā£©µÄÅäĮĻ±Č
c£®ŹŹµ±Éżøß·“Ó¦ĪĀ¶ČŗĶ½Į°čĖŁ¶Č
d£®Ļņ·“Ó¦Ę÷ÖŠ¼ÓĖ®ÖĮI2Č«²æČܽā
£Ø2£©²½Öč¢ņ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£»ÓĆpHŹŌÖ½²ā¶ØČÜŅŗpHµÄ·½·ØŹĒ
£Ø3£©²½Öč¢óŠ”ŠÄ”°Öó·Š”±Ō¼20·ÖÖÓ£¬æÉŹ¹Fe£ØOH£©2æÅĮ£³¤“ó£¬ĘäÄæµÄŹĒ£»²½ÖčV¼ÓČė»īŠŌĢæµÄÄæµÄŹĒ £®
£Ø4£©“Ó¹żĀĖ2ĖłµĆĀĖŅŗÖŠ»ńµĆBaI22H2O£ØČܽā¶ČĒśĻßČēĶ¼2ĖłŹ¾£©µÄ·½·ØŹĒ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶ¼1ŗĶĶ¼2ŹĒA”¢BĮ½ÖÖĪļÖŹµÄŗĖ“Ź²ÕńĒāĘ×”£ŅŃÖŖA”¢BĮ½ÖÖĪļÖŹ¶¼ŹĒĢžĄą£¬¶¼ŗ¬ÓŠ6øöĒāŌ×Ó”£Ēėøł¾ŻĶ¼1ŗĶĶ¼2Į½ÖÖĪļÖŹµÄŗĖ“Ź²ÕńĒāĘ×Ę×Ķ¼Ń”Ōń³öæÉÄÜŹōÓŚĶ¼1ŗĶĶ¼2µÄĮ½ÖÖĪļÖŹŹĒ
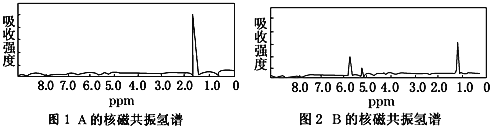
A. AŹĒC3H6£»BŹĒC6H6 B. AŹĒC2H6£»BŹĒC3H6
C. AŹĒC2H6£»BŹĒC6H6 D. AŹĒC3H6£»BŹĒC2H6
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ4ÖÖĢ¼¼ÜČēĶ¼µÄĢž£ØŠ”ŗŚĒņ±ķŹ¾Ģ¼Ō×Ó£¬ŗŚĒņÖ®¼äµÄĮ¬Ļß±ķŹ¾¹²¼Ū¼ü£©£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
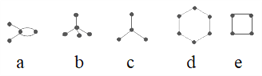
¢ŁaŗĶe»„ĪŖĶ¬·ÖŅģ¹¹Ģå ¢ŚbŹĒĢģČ»ĘųµÄÖ÷ŅŖ³É·Ö ¢ŪdĪŖĘ½ĆęŠĶ·Ö×Ó£¬ŹōÓŚ·¼ĻćĢž ¢ÜbŗĶc»„ĪŖĶ¬ĻµĪļ ¢Ża”¢d”¢eµÄ×ī¼ņŹ½ĻąĶ¬
A. ¢Ł¢Ū¢Ż B. ¢Ł¢Ś¢Ū C. ¢Ś¢Ū¢Ü D. ¢Ł¢Ü¢Ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ²»ŹōÓŚĢ¼Ō×ӳɼüĢŲµćµÄŹĒ(””””)
A.Ņ׏§Č„×īĶā²ćµÄµē×ÓŠĪ³ÉĄė×Ó
B.×īĶā²ćµē×ÓŅ×ÓėĘäĖūŌ×ÓµÄĶā²ćµē×ÓŠĪ³É¹²ÓƵē×Ó¶Ō
C.Äܹ»ŠĪ³Éµ„¼ü”¢Ė«¼üŗĶČż¼üµČ¶ąÖֳɼüŠĪŹ½
D.ĆæøöĢ¼Ō×Ó×ī¶ąÓėĘäĖūŌ×ÓŠĪ³É4øö¹²¼Ū¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ·Ö×ÓŹ½±ķŹ¾µÄĪļÖŹ£¬¾ßÓŠĶ¬·ÖŅģ¹¹ĢåµÄŹĒ(””””)
A.C3H7Cl
B.C3H8
C.CH2Cl2
D.CH4O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹæÉÓĆÓŚ“¦ĄķŠ¹Ā¶µÄÓŠ¶¾ĪļÖŹNa2SµÄŹĒ( )
¢ŁĢś·Ū ¢ŚKI ¢ŪĖ«ŃõĖ® ¢Ü³ōŃõ(O3) ¢ŻNaCl
A.¢Ł¢ŚB.¢Ū¢ÜC.¢Ł¢ŻD.¢Ū¢Ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·“Ó¦A(g)+B(g) ![]() C(g) +D(g) ·¢Éś¹ż³ĢÖŠµÄÄÜĮæ±ä»ÆČēĶ¼£¬”÷H ±ķŹ¾·“Ó¦µÄģŹ±ä”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
C(g) +D(g) ·¢Éś¹ż³ĢÖŠµÄÄÜĮæ±ä»ÆČēĶ¼£¬”÷H ±ķŹ¾·“Ó¦µÄģŹ±ä”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )

A. ·“Ó¦ĢåĻµÖŠ¼ÓČė“߻ƼĮ£¬·“Ó¦ĖŁĀŹŌö“ó£¬E1¼õŠ”£¬E2Ōö“ó
B. ·“Ó¦ĢåĻµÖŠ¼ÓČė“߻ƼĮ£¬·“Ó¦ĖŁĀŹŌö“󣬔÷HŌö“ó
C. ”÷H < 0£¬·“Ó¦“ļµ½Ę½ŗāŹ±£¬ÉżøßĪĀ¶Č£¬AµÄ×Ŗ»ÆĀŹ¼õÉŁ
D. ”÷H > 0£¬·“Ó¦“ļµ½Ę½ŗāŹ±£¬Ōö“óŃ¹Ē棬AµÄ×Ŗ»ÆĀŹ²»±ä
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com