
【题目】实验室里需要纯净的氯化钠晶体,但现在只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:
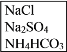
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
请回答下列问题:
(1)操作①加热的目的是________________,
(2)操作②除用BaCl2溶液外,还可用____________替代。
(3)操作②,判断SO42-已除尽的方法是________________________。
(4)操作③的目的是____________,不先过滤后再加Na2CO3溶液的理由是____________。
(5)操作④的名称是______________,应在________(填仪器名称)中进行。
【答案】加热分解除去NH4HCO3 Ba(OH)2溶液 取上层清液加入BaCl2溶液,若无沉淀说明SO42-已除尽 除去过量的Ba2+ 减少一次过滤操作 蒸发结晶 蒸发皿
【解析】
(1)化合物中碳酸氢铵受热分解分析;
(2)操作②是沉淀硫酸根离子的作用,也可以加入氢氧化钡溶液,注意不能引入新的杂质;
(3)判断SO42-已除尽选择的试剂是BaCl2溶液;
(4)操作③是除去过量的钡离子;
(5)操作④是蒸发氯化钠溶液得到氯化钠晶体,溶液蒸发在蒸发皿中加热进行。
(1)操作①加热的目的是利用碳酸氢铵受热分解生成氨气、二氧化碳、水蒸气除去碳酸氢铵固体;故答案为:加热分解除去NH4HCO3;
(2)操作②是完全沉淀硫酸根离子,原则是加入的试剂不能引入新的杂质,或最后易于除去,除了用BaCl2溶液外,也可以用Ba(OH)2溶液;
(3)操作②,判断SO42-已除尽的方法是取上层清液加入BaCl2溶液,若无沉淀说明SO42-已除尽;
(4)操作③是加入碳酸钠溶液,目的是除去过量的钡离子,避免引入钡离子杂质;所以加入碳酸钠的目的是除去过量的Ba2+;不先过滤后再加Na2CO3溶液的理由是减少一次过滤操作;
(5)操作④将溶液蒸发结晶得到溶质晶体;操作④是将氯化钠溶液蒸发结晶得到氯化钠晶体,溶液蒸发应在蒸发皿中加热进行。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子中,在碱性溶液里能大量共存,并且溶液为无色透明的是( )
A.K+ MnO4- Cl- SO42-B.Na+ K+ Al3+ Ba2+
C.Na+ HCO3- NO3- SO42-D.Na+ SO42- S2- Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物材料衍生物2,5-呋喃二甲酸(![]() )可以替代化石燃料衍生物对苯二甲酸,与乙二醇合成材料聚2,5-呋喃二甲酸乙二醇酯(PEF)。下列说法正确的是
)可以替代化石燃料衍生物对苯二甲酸,与乙二醇合成材料聚2,5-呋喃二甲酸乙二醇酯(PEF)。下列说法正确的是
A. 合成PEF的反应为加聚反应
B. PEF不能与氢气发生加成反应
C. 通过红外光谱法测定PEF的平均相对分子质量,可得其聚合度
D. 聚对苯二甲酸乙二醇酯的结构简式为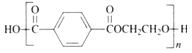
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冰晶石(Na3AlF6)微溶于水,工业上用萤石(CaF2含量为96%)、二氧化硅为原料,采用氟硅酸钠法制备冰晶石,其工艺流程如下:
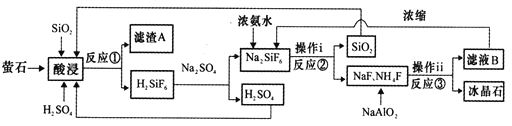
(1)Na3AlF6中氟、铝以共价键结合,写出Na3AlF6中所含阳离子的电子式________________,滤渣A的主要成分是_______________________(填名称)。
(2)为探究适合“酸浸”的条件,取4份相同样品进行实验,所得结果如下表所示:
实验编号 | 萤石品位 | 硫酸的 | 反应温度/℃ | 获得 Na2SiF6的质量 |
(CaF2含量) | 质量分数 | |||
1 | 96% | 25% | 60~70 | 120 |
2 | 96% | 35% | 60~70 | 153 |
3 | 96% | 35% | 80~90 | 100 |
4 | 96% | 40% | 60~70 | 141 |
①实验3比实验2获得Na2SiF6的质量低的原因可能是___________________。
②选择“酸浸”时所采用的最适合条件为____________________________。
(3)写出反应③的离子方程式:______________________________。
(4)“操作ⅰ”不能用硅酸盐质设备进行分离的原因__________________________。
(5)经测定,操作ⅰ所得滤液中所含杂质中K+浓度为0.05mol·L-1,当Na+浓度降为0.01mol·L-1时,若不考虑其它离子影响和溶液体积变化,K+___________(填“是”或“否”)开始沉淀。(已知25℃时,Ksp(Na3AlF6)=4.0×10-10,Ksp(K3AlF6)=6.0·10-8)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行下列实验:将①中的浓硫酸滴入②中,预测的现象与结论相符的是( )
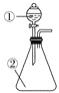
A. 若②为浓盐酸;产生大量气体产生;说明硫酸的酸性比盐酸强
B. 若②为铜片;有气泡产生,底部生成灰白色固体;说明浓硫酸有强氧化性
C. 若②为蓝色硫酸铜晶体;蓝色晶体变为白色;说明浓硫酸有吸水性,发生物理变化
D. 若②为蔗糖;白色固体变为黑色海绵状,有气体放出;说明浓硫酸有脱水性、氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中的每一方格表示相关的一种反应物或生成物。其中B是一种单质,其余物质也都是含有B元素的化合物。C是一种钠盐,E是C对应的酸,B的结构类似金刚石,D为氧化物。
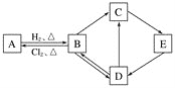
请回答下列问题:
(1)A、D、E的化学式分别为________、________、________。
(2)A和B的互相转化在工业上有什么实际意义?_____________________。
(3)写出D→C反应的化学方程式:_____________________。
(4)写出E→D反应的化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列有关电解质溶液的说法正确的是( )
A. 将Na2CO3溶液用水稀释后,pH变大,Kw不变
B. 向有AgCl固体的饱和溶液中加少许水,c(Ag+)和Ksp(AgCl)都不变
C. pH=4.75浓度均为0.1mol/L的CH3COOH、CH3COONa的混合溶液中:c(CH3COO-)+c(OH-)<c(H+)+c(CH3COOH)
D. 分别用pH=2和pH=3 的 CH3COOH溶液中和等物质的量的NaOH,消耗CH3COOH溶液的体积分别为Va和Vb,则10Va=Vb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两份铝屑,第一份与过量的盐酸反应,第二份与过量的氢氧化钠溶液反应,产生氢气的体积比为1∶2,则第一份与第二份铝屑的质量比为( )
A.1∶1B.1∶2C.1∶3D.1∶4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com