
科学家预测原子序数为114的元素具有相当稳定的核素,它在元素周期表中的位置在第7周期ⅣA族,位于铅的下方,称为类铅。下列关于它的性质叙述中,错误的是( )
A.它的最高价氧化物的水化物是强酸 B.它的金属性比铅强
C.它具有7个电子层 D.它的最外层电子数为4
 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.1molSiO2晶体内含有2NA个Si—O键
B.在0.1mol熔融KHSO4中,含有0.1NA个SO42-
C.在0.5L 1mol·L-1的盐酸中所含粒子总数为NA
D.1molSi晶体内含有2NA个Si—Si键
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期的两种元素A和B,它们的离子A-和B2+具有相同的电子层结构,下列说法中正确的是 ( )
A、原子序数A>B B、电子总数A>B
C、离子半径A->B2+ D、原子半径A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
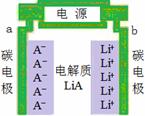
正、负极都是碳材料的双碳性电池,电池充、放电过程为2nC+LiA  CnA+LiCn,充电时Li+、A-分别吸附在两极上形成LiCn和CnA(如图所示),下列说法正确的是( )
CnA+LiCn,充电时Li+、A-分别吸附在两极上形成LiCn和CnA(如图所示),下列说法正确的是( )
A.a是电池的负极
B.放电时,A-离子向b极移动
C.放电时,负极的电极反应式是nC-e-+A-= CnA
D.充电时,电解质中的离子浓度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表揭示了化学元素间的内在联系,使其构成了一个完整的体系。
(1)第二周期元素碳、氮、氧的电负性从大到小顺序为 (用元素符号表示)。
(2)第四周期元素砷、硒、溴的第一电离能从大到小顺序为
(用元素符号表示)。
(3)第 IIIA族元素原子具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质。
①[B(OH)4]-中B的原子杂化类型为 ;
②不考虑空间构型,[B(OH)4]-的结构可用示意图表示为 。
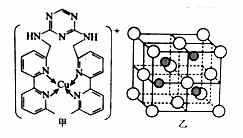 (4)过渡区元素铜的离子是人体内多种酶的辅因子。某化合物Y 与Cu(Ⅰ)(Ⅰ表示化合价为+1)结合形成图甲所示的离子:
(4)过渡区元素铜的离子是人体内多种酶的辅因子。某化合物Y 与Cu(Ⅰ)(Ⅰ表示化合价为+1)结合形成图甲所示的离子:
①写出Cu(Ⅰ)的电子排布式 ;
②该离子中含有化学键的类型有 (选填字母)。
A.极性键 B.离子键 C.非极性键 D.配位键
③向氯化铜溶液中通入足量的二氧化硫,生成白色沉
淀M,M的晶胞结构如图乙所示。写出该反应的
离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来,科学家发现一种新分子,它具有空心的类似足球状结构,化学式为C60 。下列说法中,正确的是( )
A.C60是一种新型化合物 B.C60属于原子晶体
C.C60在纯氧中燃烧只生成一种产物CO2 D.C60的相对分子质量为720
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组性质的比较,正确的是( )
A.原子半径:Na< Mg < Al B.酸性强弱:H2CO3 < H2SiO3 < HNO3
C.热稳定性:HF > HCl > HBr D.非金属性强弱:P > S > Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com