
| 选项 | 实验方案 | 现象 | 结论 |
| A | 向SiO2固体中加入足量盐酸 | 固体不溶解 | SiO2不溶于任何酸 |
| B | 向Na2CO3溶液中通入足量CO2 | 产生晶体 | 溶解度:NaHCO3>Na2CO3 |
| C | 向75%的酒精中加入小粒钠 | 产生气泡 | 乙醇与钠反应产生H2 |
| D | 向KI 淀粉溶液中通入气体X | 溶液变蓝 | X的氧化性比I2的氧化性强 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二氧化硅与盐酸不反应;
B.Na2CO3溶液不一定为饱和溶液;
C.钠与水、乙醇均反应生成氢气;
D.溶液变蓝可知生成碘.
解答 解:A.二氧化硅与盐酸不反应,与HF酸反应,故A错误;
B.Na2CO3溶液不一定为饱和溶液,若为饱和溶液,通入足量CO2,析出晶体可知溶解度:NaHCO3<Na2CO3,故B错误;
C.钠与水、乙醇均反应生成氢气,不能说明乙醇与钠反应产生H2,故C错误;
D.溶液变蓝可知生成碘,则X的氧化性比I2的氧化性强,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、反应与现象、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 硝酸铵 | B. | 氯化钠 | C. | 生石灰 | D. | 蔗糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下5.6L CH4含有的共用电子对数目为NA | |
| B. | 25℃时,pH=1的硫酸溶液中含有H+的数目为0.1NA | |
| C. | 常温下,23g NO2和N2O4混合气体中所含原子总数为1.5NA | |
| D. | 将0.5mol NH4NO3于稀氨水使溶液呈中性,溶液中NH4+数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 原子或分子相关信息 | 单质及其化合物相关信息 | |
| X | ZX4分子是由粗Z提纯Z的中间产物 | X的最高价氧化物对应的水化物为无机酸中最强酸 |
| Y | Y原子的最外层电子数等于电子层数 | Y的氧化物是典型的两性氧化物,可用于制造一种高温材料 |
| Z | Z原子的最外层电子数是次外层电子数的$\frac{1}{2}$ | Z广泛存在于无机非金属材料中,其单质是制取大规模集成电路的主要原料 |
| W | W原子的最外层电子数小于4 | W的常见化合价有+3、+2,WX3稀溶液呈黄色 |
 ;X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为6H++Al2O3=2Al3++3H2O.
;X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为6H++Al2O3=2Al3++3H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水,产生黄绿色气体:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2+Cl2 | |
| B. | 用Na2CO3溶液将水垢中的CaSO4转化为CaCO3:CO32-+Ca2+=CaCO3 | |
| C. | 向H202溶液中滴加CuSO4溶液,产生气泡:2H2O2 $\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2 T | |
| D. | 向苯酚浊液中滴加Na2CO3溶液,溶液变澄清: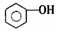 +CO32-→ +CO32-→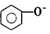 +HCO3- +HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人工合成的硅橡胶是目前最好的既耐高温又耐低温的橡胶 | |
| B. | 肥皂水显碱性,可用作蚊虫叮咬处的清洗剂 | |
| C. | 明矾净水是因为明矾水解产生的氢氧化铝胶体可以吸附水里悬浮的杂质 | |
| D. | 铝比铁更活泼,铁制品比铝制品更耐腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2NA | |
| B. | 将1 mol Cl2通入水中,HC1O、Cl-、ClO-粒子数之和为2NA | |
| C. | 标准状况下,44.8L NO与22.4 L O2反应后的分子数是2NA | |
| D. | 27g铝中加入1mol/L的NaOH溶液,转移电子数是3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
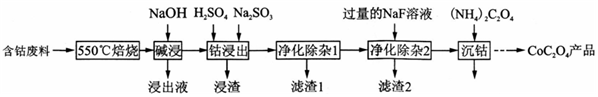
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 如图的键线式表示烃的名称为3-甲基-4-乙基-7-甲基辛烷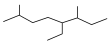 | |
| B. | 符合分子式为C3H8O的醇有三种不同的结构 | |
| C. | 乙烯在一定条件下能发生加成反应、加聚反应,被酸性高锰酸钾溶液氧化,也能在一定条件下被氧气氧化成乙酸 | |
| D. | 溴水能将 甲苯、乙烯、乙醇、四氯化碳、乙酸五种溶液鉴别开来 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com